卵巢癌是严重威胁妇女健康的恶性肿瘤之一,发病率在女性生殖系统恶性肿瘤中位居第3位。既往卵巢癌的主要治疗模式是手术-化疗-随访-复发-再治疗-随访。尽管晚期卵巢癌患者对铂类药物和紫杉醇联合化疗的初始反应率很高,但随着时间的推移,治疗的有效性会降低,70%的患者在3年内会复发[1]。
以尼拉帕利为代表的PARP抑制剂的出现,为卵巢癌治疗带来革命性变化。大量高级别临床证据显示,基于PARP抑制剂的维持治疗不仅显著延长患者无进展生存期,降低复发风险,还可帮助患者保有较好的生活质量,并为数十年来一直没有得到实质性改善的卵巢癌5年生存率的提高燃起新的希望[2]。
2021年6月,国家医疗保障局起草并向社会公布了“国家医保药品目录调整工作方案”[3]。这一消息很快引起了临床医生和卵巢癌患者的广泛关注。如何尽快将尼拉帕利适用于全人群一线维持治疗的新适应证纳入医保目录,藉此更好地改善临床治疗,造福广大患者,已成为医患的热切期盼。
尼拉帕利开启卵巢癌全人群一线维持治疗新时代
维持治疗是指在完成既定的化疗周期数,肿瘤得到最大程度缓解后,再延长治疗使患者保持受益的治疗方法。维持治疗的概念其实并不新鲜,现已成为非小细胞肺癌、多发性骨髓瘤、急性淋巴细胞白血病、结肠癌等多种肿瘤治疗的重要组成部分。
对于卵巢癌的维持治疗,临床研究人员曾经做过多次探索和尝试,采用了包括化疗、放疗及免疫治疗在内的多种手段,但均未取得成功。这一难题直到PARP抑制剂出现后,方才迎来了转机。
PARP在DNA单链碱基切除、修复过程中发挥关键作用。在HRD肿瘤细胞中DNA双链无法修复,PARP抑制剂又阻断单链修复,从而形成“合成致死”效应,导致肿瘤细胞死亡。此外,PARP抑制剂能够捕获DNA单链断裂位点处的PARP,使PARP无法从与DNA断裂位点处解离,从而阻断后续DNA的修复。
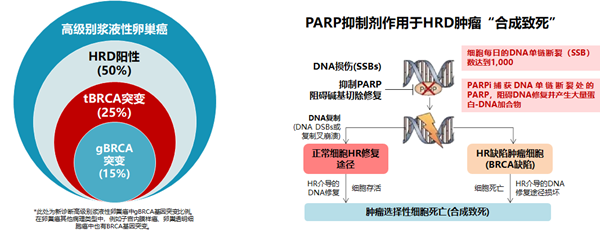
图1. PARP抑制剂作用机制
作为PARP抑制剂中的佼佼者,尼拉帕利不仅是国家1类新药,而且在研发过程中两次荣获国家“十三五”“重大新药创制”重大科技专项的支持。该药物于2019年12月获得NMPA批准用于铂敏感的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在含铂化疗达到完全缓解或部分缓解后的维持治疗。目前这一适应证已于2020年12月被纳入国家医保目录。
2020年9月,尼拉帕利再传捷报,NMPA批准其用于一线含铂化疗完全或部分缓解的所有(不论其生物标志物状态如何)上皮性卵巢癌、输卵管癌或原发性腹膜卵巢癌成人患者维持治疗。这一批准决定使得尼拉帕利成为唯一一款突破BRCA局限,将卵巢癌一线维持治疗的阵地拓展至全人群的PARP抑制剂。
而今,凭借着独特的作用机制、卓越的有效性和安全性表现以及广泛的适用人群,尼拉帕利从已获批上市的PARP抑制剂中脱颖而出,正在赢得越来越多医患的认可。
尼拉帕利全人群一线维持治疗疗效卓越
2019年于ESMO年会上公布,并同步发表在顶尖医学期刊《新英格兰医学杂志》上的双盲、随机、安慰剂对照3期临床试验PRIMA研究[4]第一次证实,无论生物标志物状态如何,尼拉帕利均能显著改善卵巢癌患者的PFS。这一坚实证据一举打破了只有BRCA突变卵巢癌患者才能从PARP抑制剂一线维持治疗中获益的僵局。
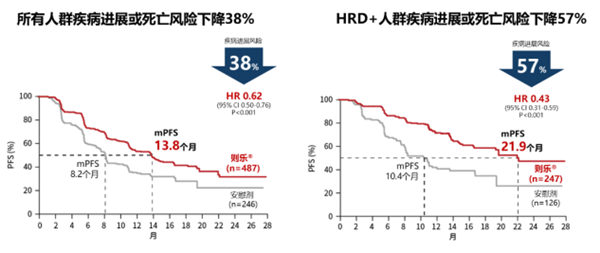
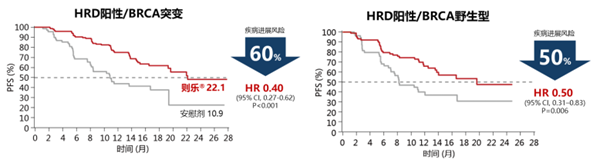
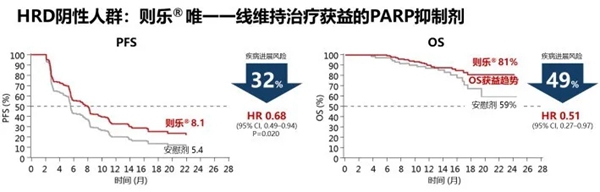
图2:尼拉帕利助力卵巢癌一线维持治疗进入全人群时代
从整体来看,与安慰剂相比,尼拉帕利可显著延长全体人群的无进展生存期至13.8个月,降低38%的疾病进展或死亡风险。在HRD阳性患者组,尼拉帕利表现更加优异,可显著延长PFS至21.9个月,降低57%的疾病进展或死亡风险。
进一步分析发现,HRD+/BRCA突变的患者可以从尼拉帕利一线维持治疗中获益更多,PFS达到22.1个月,降低疾病进展或死亡风险60%;对于HRD+/BRCA野生型患者,尼拉帕利也可延长PFS至19.6个月,降低疾病进展或死亡风险50%。值得注意的是,即使是HRD阴性亚组也能获益,尼拉帕利可使PFS延长至8.1个月,降低疾病进展或死亡风险32%。
尼拉帕利的强效源于其强效捕获,生物利用高以及药物相互作用少等独特药理特性
尼拉帕利之所以有此疗效,与它的独特药理特性息息相关[5][6]。
高PARP捕获(trapping)活性:与其他PARPi相比,尼拉帕利具有更强的PARP捕获活性,有利于其在BRCAwt患者中发挥良好抗肿瘤疗效。
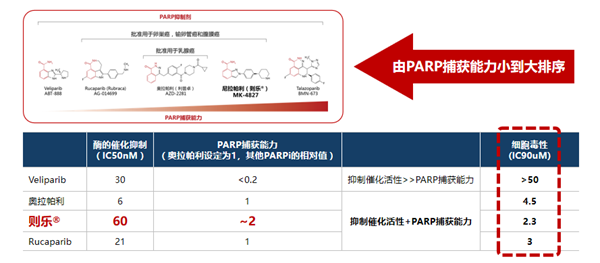
生物利用度高,药物相互作用少:尼拉帕利生物利用度高达73%,更容易被吸收;长达36小时的半衰期,只需口服一天一次;独特的羧酸酯酶代谢,有较少药物相互作用。
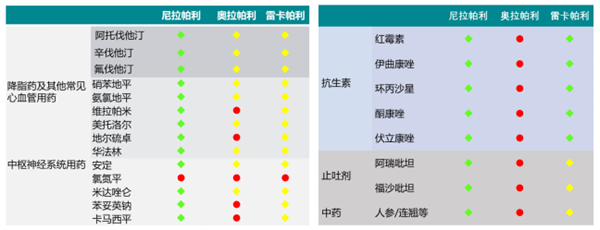
(*:以上信息来自于药品说明书对药物代谢途径的描述,并非所有药物都进行了药物相互作用的PK实验,红色图标为说明书中提及的避免联合应用的药物,黄色图示代表共用相关代谢途径可能导致药物浓度变化,提醒注意剂量检测及调整;绿色表示不共用代谢途径,预期无明显的相互作用。)
在肿瘤/血浆/脑组织中暴露量高:尼拉帕利具有较高的生物利用度和表观分布容积,使得其在肿瘤药物暴露量高,能够很好地穿透血脑屏障。这也是尼拉帕利对BRCA突变、BRCA野生型HRD阳性、HRD阴性卵巢癌均有效的原因之一。
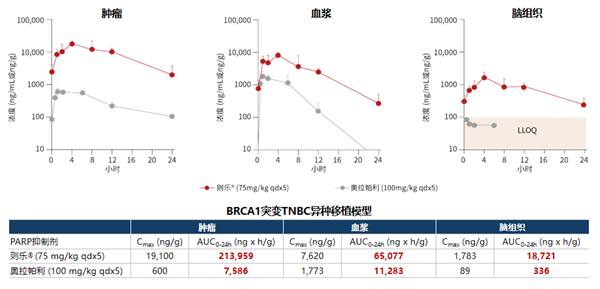
尼拉帕利长期用药耐受性好,终止率低,个体化起始剂量为用药安全保驾护航,更适合中国人群
维持治疗需要长期用药,对药物的安全性有着较高要求。从已有的研究数据来看,尼拉帕利与其他PARP抑制剂相似,其不良反应主要与消化系统和血液系统相关。
消化系统不良反应主要为恶心、呕吐等,一般患者能够耐受,若反应较重,临床可对症治疗。血液系统相关不良反应包括血小板下降和贫血,大多为1-2级。综合看来,只要及时对症处理或进行剂量调整,这些不良反应均能得到有效控制。
值得一提的是,以中国人群为研究对象的NORA研究[7]首次前瞻性验证了尼拉帕利个体化起始剂量在铂敏感复发患者维持治疗的有效性和安全性。基于这一结果,根据患者基础体重和/或基线血小板计数对尼拉帕利起始剂量进行调整,不仅不会影响疗效,而且进一步提高了药物的安全性(3/4级血小板减少降低2倍,NORA研究中尼拉帕利的终止率仅为4%)。
尼拉帕利新适应证纳入医保众望所归
当下,PARP抑制剂的疗效已得到广大医生和患者的充分认可,并获得众多国际、国内指南推荐,国家医疗保障局亦积极响应医患需求,将部分适应证纳入到医保目录。目前携带BRCA突变的患者使用PARP抑制剂一线维持治疗业已得到国家医保的支持,但该部分患者仅占卵巢癌全人群的25%,意味着大部分患者在进行维持治疗时,仍然面临沉重的医疗负担。
此外,第三方调研数据发现,卵巢癌一线维持治疗比例较低,即使进行一线维持治疗的患者中还有很大比例的患者没有规范用药。尼拉帕利用于全人群一线维持治疗的适应证已获批准,将其纳入医保目录的呼声日益强烈。如果此次医保目录调整能够将尼拉帕利的这一适应证纳入保障序列,那些需要进行一线维持治疗而未进行的患者,以及未规范使用药物进行一线维持的患者有望在国家医保的支持下,受益于尼拉帕利带来的更长生存和更好生活质量。
期待这一天能够尽早到来!
参考资料:
[1]李艺, 崔恒. 重视卵巢癌的维持治疗[J]. 中国妇产科临床杂志, 2019, v.20(05):7-9.
[2]中国抗癌协会妇科肿瘤专业委员会. 卵巢恶性肿瘤诊断与治疗指南(2021年版)[J].中国癌症杂志, 2021, 31(6): 474-484.
[3]http://www.nhsa.gov.cn/module/download/downfile.jsp?classid=0&filename=46f93e617b854eb19fb1106ab3e3765f.pdf
[4]GONZáLEZ-MARTíN, A, POTHURI B, VERGOTE I, et al.Niraparib in Patients with Newly Diagnosed Advanced OvarianCancer[J]. N Engl J Med, 2019, 381(25):2391-2402.
[5]Sandhu S K , Schelman W R , Wilding G , et al. The poly(ADP-ribose) polymerase inhibitor niraparib (MK4827) in BRCA mutation carriers and patients with sporadic cancer: a phase 1 dose-escalation trial.[J]. Lancet Oncology, 2013, 14(9):882-892.
[6]Wang D , Zou L , Jin Q , et al. Human carboxylesterases: a comprehensive review[J]. 药学学报(英文版), 2018, 008(005):699-712.
[7]Wu X H, Zhu J Q, Yin R T, et al. Niraparib maintenance therapy in patients with platinum-sensitive recurrent ovarian cancer using an individualized starting dose (NORA): a randomized, double-blind, placebo-controlled phase III trial☆[J]. Annals of Oncology, 2021, 32(4): 512-521.

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
