2020年ASCO大会上,复旦大学附属中山医院臧荣余教授首次在口头报告专场公布了SOC-1研究的结果。与德国III期DESKTOP研究互相印证,SOC-1研究再次证实,二次肿瘤细胞减灭术可为铂敏感复发性卵巢癌患者带来无进展生存期(PFS)获益。近日,SOC-1研究全文发表于The Lancet Oncology[1]。

研究背景
约80%晚期卵巢癌患者一线化疗和靶向维持治疗后会复发。二次肿瘤细胞减灭术临床应用广泛,但其是否可用于铂敏感复发性卵巢癌仍备受争议。
近年研究显示,二次肿瘤细胞减灭术可以改善预后,延长患者生存。但由于卵巢癌复发时常发生盆、腹腔内广泛转移,通过手术将癌灶全部清除对手术医生提出了极高的要求,完全二次手术(R0)很难做到;而未达到完全切除(R1/R2)的手术对卵巢癌的治疗不利,这也是多数复发性卵巢癌患者不能从手术获益的主要原因。
因此,需要有效的评分系统筛选适合手术的患者。目前国际上已有的较为系统和成熟的评分系统有两个,其一为德国妇科肿瘤临床研究协作组(AGO)提出的AGO评分系统(II期DESKTOP研究中得到验证)[2];其二即为复旦大学附属中山医院臧荣余教授团队提出的复发性卵巢癌iMODEL (国际合作拟合模型)风险评分系统。
越来越多的证据显示,18氟-氟代脱氧葡萄糖(18F-FDG)PET/CT可预测复发性卵巢癌完全切除的敏感性和特异性。臧荣余教授团队将iMODEL评分与PET-CT成像结合,建立了新型评分系统和患者选择标准,以筛选能从二次肿瘤细胞减灭术中获益的合适患者。
目前,有三项关于二次肿瘤细胞减灭术的随机对照研究:AGO DESKTOP(德国)、GOG-0213(美国)、上海妇科肿瘤协作组(SGOG)SOC-1(中国),旨在探索二次肿瘤细胞减灭术是否可成为复发性卵巢癌患者的标准治疗。
SOC-1研究于2011年正式开展,旨在确认对复发性卵巢癌进行二次肿瘤细胞减灭术的疗效与安全性。本研究中,臧荣余教授团队公布了SOC-1研究的PFS结果和预设的OS中期分析结果,并首次分析了累积无治疗生存时间(accumulating treatment-free survival,TFSa)。
研究方法
SOC-1是一项在中国4个中心开展的开放标签、随机对照、III期临床研究。入组18岁及以上的铂敏感复发性上皮性卵巢癌患者,一线含铂治疗结束后无铂间期至少6个月,根据 iMODEL评分结合 PET-CT 检查结果预测为复发病灶可完全切除。iMODEL评分由6个变量(FIGO 分期、初次手术后残留病灶、无铂间期、ECOG PS评分、复发时血清CA125水平、腹水)得分相加而来,总体上iMODEL评分≤4.7分提示完全切除的可能性更高。
符合条件的患者按1:1比例随机分配接受二次肿瘤细胞减灭术序贯化疗(静脉注射紫杉醇[175 mg/m2]或多西他赛[75 mg/m2],6个周期,每3周一次)(手术组)联合卡铂(5 mg/ml/min)或仅化疗(无手术组)。共同主要终点为PFS和OS,次要终点为TFSa。
研究结果
2012年7月19日至2019年6月3日期间,研究共纳入357例患者,并随机分配到手术组(n=182)和无手术组(n=175),两组最终分别纳入172例和158例患者(图1)。患者基线特征见表1。
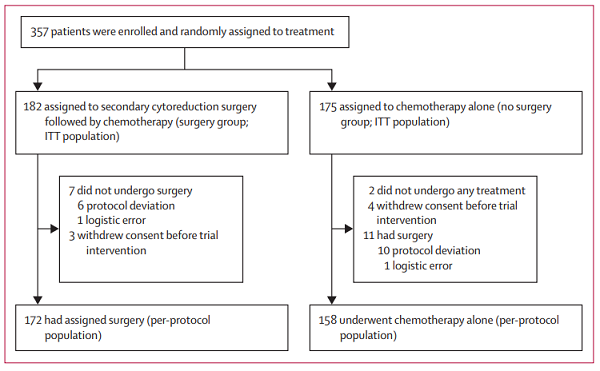
图1 试验流程图
表1 患者基线特征
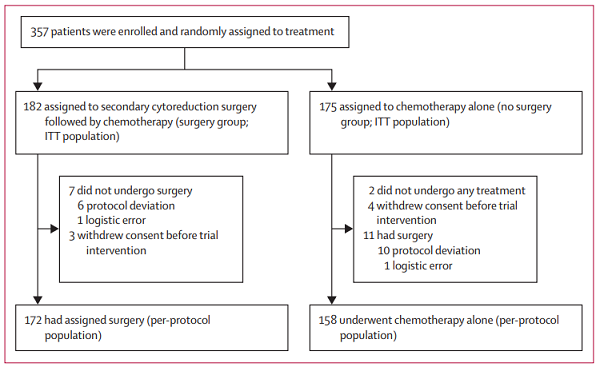
2019年12月17日数据库锁定时,无手术组中有130例患者复发。手术组和无手术组的中位随访时间分别为36个月和33.9个月,两组的中位PFS分别为17.4个月和11.9个月(HR=0.58,P<0.0001,图2),两组的2年PFS率分别为38%和22%。事后亚组分析见图3。
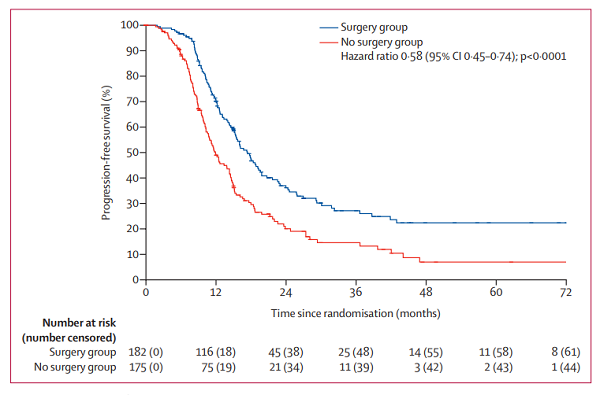
图2 ITT人群PFS分析结果
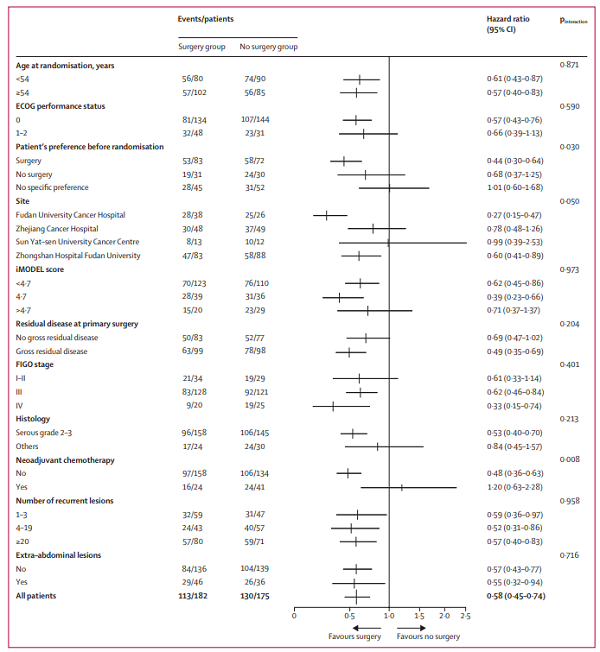
图3 亚组分析结果
手术组和无手术组的中位OS分别为58.1个月和53.9个月(HR=0.82),OS结果尚不成熟,仍需进一步随访。两组中位至首次后续抗肿瘤治疗时间分别为18.1个月和13.6个月(HR=0.59),两组中位至第二次后续抗肿瘤治疗时间分别为33.5个月和28.1个月(HR=0.69)。
手术组和无手术组的中位TFSa分别为46.8个月和42.4个月。
手术组的完全切除率为77%(132/177)。iMODEL评分大于4.7的患者被分配至接受手术,完全切除率为61%;相比之下,iMODEL评分小于4.7的154例患者被分配接受手术,完全切除率为79%。
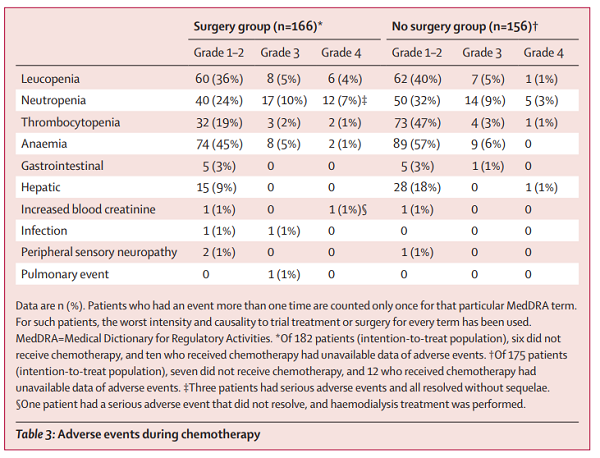
手术组中,30天时,有9例(5%)患者发生3级或以上手术并发症(表2)。化疗期间最常见的3-4级不良事件是中性粒细胞减少(手术组[17%] vs无手术组[12%])、白细胞减少(9% vs 6%)和贫血(6% vs 6%)(表3)。
表2 手术组30天时并发症
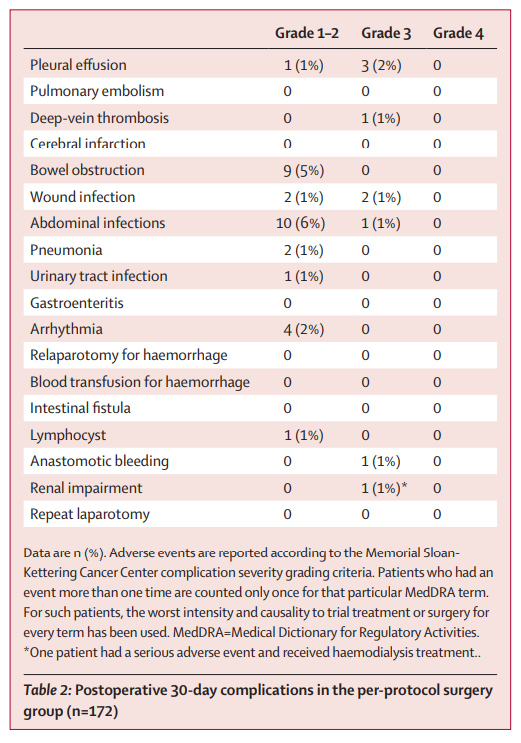
表3 安全性分析
讨论与结论
结果显示,与单独化疗相比,二次肿瘤细胞减灭术序贯化疗与铂敏感复发卵巢癌患者PFS延长相关,患者应积极在特定医学中心咨询是否可接受二次肿瘤细胞减灭术。与III期DESKTOP研究最终分析类似(PFS HR=0.66),SOC-1研究显示,二次肿瘤细胞减灭术+化疗可延长患者PFS达5.6个月(HR=0.58)。
至首次和第二次后续抗肿瘤治疗时间是PFS和OS之间的关键节点,二次肿瘤细胞减灭术+化疗的至首次和第二次后续抗肿瘤治疗均长于单独化疗组。
该研究结果创新了复发卵巢癌的诊疗模式,为铂敏感复发性卵巢癌二次肿瘤细胞减灭术提供了更高级别循证医学证据,未来有望改变复发卵巢癌临床实践。
参考文献:
[1]Secondary cytoreduction followed by chemotherapy versus chemotherapy alone in platinum-sensitive relapsed ovarian cancer (SOC-1): a multicentre, open-label, randomised, phase 3 trial. https://doi.org/10.1016/S1470-2045(21)00006-1.
[2] Heitz F, du Bois A, Kurzeder C, Pfisterer J, Barinoff J, Grabowski J, Hilpert F, Mahner S, Harter P. Surgery for recurrent ovarian cancer. Womens Health (Lond). 2011 Sep;7(5):529-35. doi: 10.2217/whe.11.52. PMID: 21879821.

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
