2020 ESMO大会上,一项卵巢癌相关重磅中国研究惊艳亮相,被纳入LBA摘要专场。近日,该研究发表于《Annals of Oncology》杂志(IF:18.274)。这项研究即由复旦大学附属肿瘤医院吴小华教授牵头的NORA研究,是在中国30多家医院开展的一项III期研究,旨在评估尼拉帕利(个体化剂量)用于中国铂敏感复发卵巢癌患者维持治疗的疗效和安全性。
铂敏感复发性卵巢癌中国患者接受尼拉帕利(n=177)维持治疗或安慰剂治疗(n=88)。
与安慰剂相比,尼拉帕利维持治疗的中位无进展生存期(PFS)更长(18.3个月vs. 5.4个月)(HR=0.32,P< 0.0001)。
在根据体重和血小板计数接受个体化剂量的249例患者中,尼拉帕利维持治疗有类似的PFS获益。
尼拉帕利组和安慰剂组分别有50.8%和19.3%患者发生3级及以上治疗期间不良事件(TEAE)。
1、研究背景
一线含铂化疗的有效率约为80%,但大部分患者会在2年内发生疾病进展。对于铂敏感患者,二线治疗仍会考虑含铂化疗方案。但是,若持续接受化疗,其有效率会减少、缓解持续时间会缩短,而毒性会增加。
PARP抑制剂维持治疗可延长铂敏感复发卵巢癌的PFS和无化疗间隔(CFI)。尼拉帕利、奥拉帕利、rucaparib已获FDA和EMA批准用于卵巢癌的维持治疗。不论BRCA突变如何,尼拉帕利、奥拉帕利、rucaparib维持治疗均显示出疗效,而BRCA突变患者的PFS获益最大。
基于III期NOVA研究,尼拉帕利被推荐用于铂敏感复发卵巢癌患者的维持治疗。研究发现,73%患者会发生剂量减少(最初剂量为300mg/日),大部分患者会因血小板减少而在最初三个月发生剂量减少。RADAR回顾性研究发现,基线体重<77kg或血小板计数<150000/μL患者接受尼拉帕利的剂量为200mg/日,但疗效差异未知。
III期NORA研究旨在评估尼拉帕利用于铂敏感复发中国卵巢癌患者的疗效和安全性。研究期间,研究者依据基线体重和血小板计数水平采用了300或200mg起始剂量。该研究首次在中国患者评估了个体化起始剂量(ISD)尼拉帕利用于铂敏感复发卵巢癌患者维持治疗的疗效和安全性。
2、研究方法
这是一项安慰剂对照、双盲、III期随机研究,在中国30家中心开展。入组患者按2∶1比例随机分配接受尼拉帕利或安慰剂维持治疗。在采用初始固定剂量300 mg入组16例受试者后,采用尼拉帕利个体化起始剂量,对于基线体重<77 kg或血小板计数<150 000/uL者,应用起始剂量200 mg(每日1次),否则起始剂量为300 mg(每日1次)。主要终点为盲法独立中心评估(BICR)的PFS。
3、主要结果
2017年9月26日至2019年2月2日期间,共纳入265例患者,尼拉帕利组和安慰剂组分别有177例和88例(图1)。249例(94%)患者随机接受了个体化起始剂量,14例患接受了300mg尼拉帕利或安慰剂治疗(中位体重82.5kg),235例患者接受了200mg尼拉帕利或安慰剂治疗(中位体重59.0kg)。
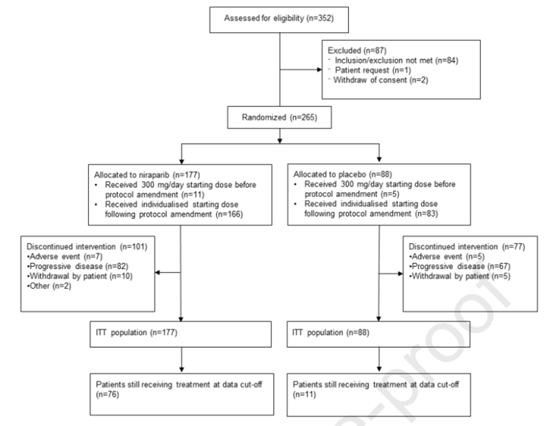
图1 试验流程图
2020年2月1日数据截止时,仍有43%和11%患者接受尼拉帕利或安慰剂治疗。中位随访时间为15.8个月。
主要研究终点
在意向治疗人群(ITT)中,与安慰剂组相比,尼拉帕利组的中位PFS明显延长(18.3个月 vs 5.4个月)(图2),PFS获益与尼拉帕利相关,而不依赖于BRCA突变状态(图3和4)。胚系BRCA突变患者尼拉帕利组的中位PFS最长,尼拉帕利组和安慰剂组的中位PFS分别为未达到和5.5个月(HR=0.22);无胚系BRCA突变患者中,尼拉帕利组和安慰剂组的中位PFS分别为11.1个月和3.9 个月(HR=0.040)。
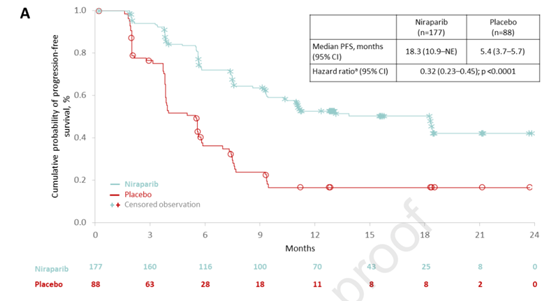
图2 ITT人群PFS结果
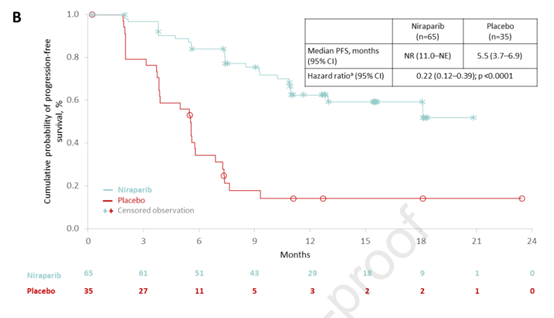
图3 胚系BRCA突变患者的PFS结果
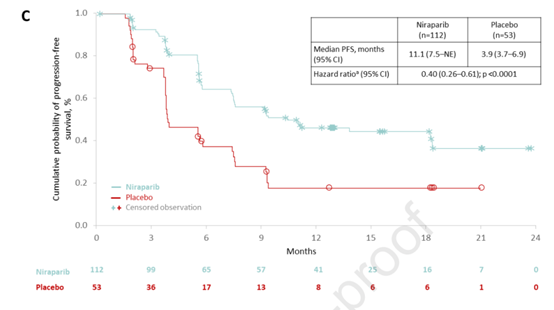
图4 无胚系BRCA突变患者的PFS结果
亚组分析显示了PFS获益的一致性(图5)。
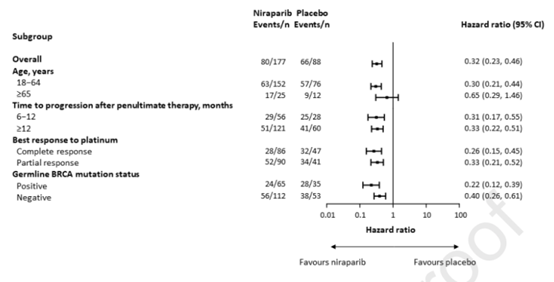
图5 亚组分析结果
次要研究终点
与安慰剂组相比,尼拉帕利组的中位CFI更长(18.5个月和9.7个月)(HR=0.34,P<0.0001)。两组的中位至第一次后续治疗时间(TFST)分别为16.7个月和7.7个月(HR=0.35,P<0.0001)。两治疗组的中位总生存期(OS)均未达到。
安全性
尼拉帕利组和安慰剂组分别有50.8%和19.3%患者发生3级及以上 TEAE。导致剂量减少的最常见的不良事件是血液学毒性,包括血小板计数减少、中性粒细胞计数减少、贫血。
4、讨论和结论
这项研究是目前唯一在亚洲患者中开展的,评估PARP抑制剂维持治疗的III期随机对照临床研究,也是首个评估PARP抑制剂维持治疗个体化给药方案的临床研究。
尼拉帕利维持治疗可明显降低铂敏感复发卵巢癌患者疾病进展或死亡风险达68%,个体化给药方案有效且安全性良好,可考虑用于临床实践。
参考文献:
Wu XH, Zhu JQ, Yin RT, Yang JX, Liu JH, Wang J, Wu LY, Liu ZL, Gao YN, Wang DB, Lou G, Yang HY, Zhou Q, Kong BH, Huang Y, Chen LP, Li GL, An RF, Wang K, Zhang Y, Yan XJ, Lu X, Lu WG, Hao M, Wang L, Cui H, Chen QH, Abulizi G, Huang XH, Tian XF, Wen H, Zhang C, Hou JM, Mirza MR. Niraparib maintenance therapy in patients with platinum-sensitive recurrent ovarian cancer using an individualized starting dose (NORA): a randomized, double-blind, placebo-controlled phase 3 trial. Ann Oncol. 2021 Jan 13:S0923-7534(21)00008-9. doi: 10.1016/j.annonc.2020.12.018. Epub ahead of print. PMID: 33453391.

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
