尼拉帕尼对中国上皮性卵巢癌患者是安全的
尼拉帕尼作为PARP抑制剂,其已被美国FDA批准用于铂敏感复发性卵巢癌的维持治疗,目前的两项大型研究(PN001和NOVA)也已证实了尼拉帕尼在白种人群中的安全性和药动学特性。因人群种族的特异性差异,尼拉帕尼是否在中国人群中也有同样的安全性和药动学特性,近期发表于The Oncologist杂志的一篇关于尼拉帕尼在中国上皮性卵巢癌患者中的相关性研究揭晓了答案。
这项研究是基于前期PN001和NOVA两项研究基础上进行的研究设计,这是一项随机的、开放性、单臂I期临床研究,共招募了36例上皮性卵巢癌中国患者,按照1:1:1的分组模式分别接受口服尼拉帕尼100 mg、200 mg、300 mg,每日一次,1个疗程28天。本研究主要目的是阐明尼拉帕尼在中国人群中的药动学特性和评价其安全性,以及是否与白种人群存在差异。
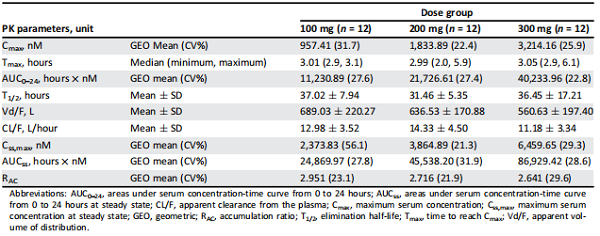
群体药动学研究分析发现,每日剂量从100 mg~300 mg,最大血清浓度(Cmax)和药时曲线下面积(AUC)会增加剂量比例,人群种族对尼拉帕尼的AUC没有影响,对Cmax的影响亦可忽略不计,另外随着基线体重的下降,尼拉帕尼的Cmax和AUC稍微增加。在分别服用100 mg、200 mg、300 mg尼拉帕尼后,血液中达到药物浓度峰值的中位时间为2.99~3.05个小时。
药物的终末消除半衰期、表观清除率、表观分布容积随着服药剂量增大仅发生轻微改变。药物平均终末消除半衰期为35个小时,与前期白种人群中的研究结果类似,且明显长于其他类型的PARP抑制剂,因此患者仅需每天服用一次药物,并且能坚持长期服用。药物表观分布容积中位数为628.3L,也明显高于其他类型PARP抑制剂,表明它有更好的肿瘤组织渗透性,从而增加对癌细胞的杀伤力。稳态累计比率(Rac)在各组中变化不大(Rac在100 mg、200 mg、300 mg组分别为2.951、2.716、2.641),几乎相一致的累计比率能导致可预见的稳态药物暴露。
表1. 中国卵巢癌患者服用尼拉帕尼药物后的药动学参数
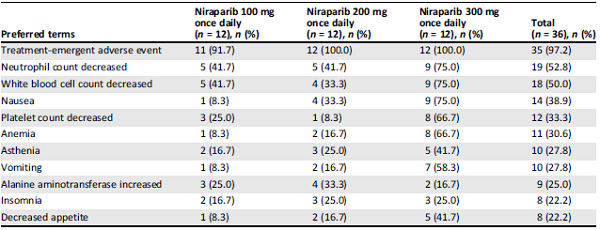
在安全性方面,36例患者中共有35例出现了至少一项治疗后不良事件(100 mg组11例,另外两组全部患者)(表2),虽然三组间的药物相关不良事件发生率类似,但300 mg组的不良事件严重程度明显高于另外两组。发生的非血液系统的常见不良反应包括:恶心、呕吐、无力、丙氨酸转氨酶增高、腹泻和食欲减退。
表2. 尼拉帕尼治疗相关的不良事件
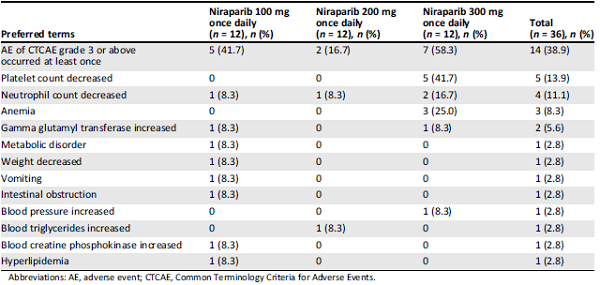
血液系统的常见不良反应包括:中性粒细胞计数减少、白细胞计数减少、血小板减少和贫血。3/4级不良反应包括:血小板减少、中性粒细胞减少、贫血和γ谷酰基转移酶增高,但通过药物治疗或者减少用药剂量,此类不良事件均能得到有效控制(表3)。未发生一例因不良事件而导致死亡的病例。
表3. 尼拉帕尼治疗相关的≥3级的不良事件
综上所述,尼拉帕尼在中国卵巢癌患者中是安全的,并且耐受性较好。
参考文献:
Jian Zhang, Hong Zheng, Yunong Gao,et al. Phase I Pharmacokinetic study of Niraparib in Chinese patients with Epithelial Ovarian Cancer.Oncologist,?2020,25(1),19-e10?DOI:?10.1634/theoncologist.2019-0565
CCNE1、BRD4和高级别浆液性卵巢癌患者预后相关
既往研究发现在同源重组高级别浆液性卵巢癌(HGSOC)患者中,CCNE1和BRD4基因是扩增的,但CCNE1和BRD4基因的扩增与HGSOC患者的临床结局的相关性仍不清楚。近期Gynecologic Oncology杂志发表的一项研究来回答这个问题。
这项研究通过美国癌症基因图谱(TCGA)数据库提取了579例HGSOC患者并检测CCNE1和BRD4扩增数据及cyclin E和BRD4蛋白表达的反向蛋白质阵列数据,免疫组化检测110例HGSOC患者实体标本cyclin E和BRD4蛋白表达情况,并分析表达情况与患者预后的相关性。
研究结果
在来源于TCGA数据库的579例HGSOC患者中,CCN1在125例(22%)患者中扩增,BRD4在98例(17%)患者中扩增,另外在这98例患者中又同时检测到47例(48%)伴CCNE1扩增。相比于二倍体肿瘤,cyclin E和BRD4蛋白表达明显增加,并且两者间存在显著相关性(r=0.23,p<0.001),免疫组化实验也得出类似结果(r=0.21,P=0.025)。在CCNE1和BRD4同时扩增的HGSOC患者,相比于无扩增的HGSOC患者,中位生存期更短(37.9个月VS 48.1个月,p=0.029)。只有CCNE1或BRD4扩增的患者与没有CCNE1或BRD4扩增的患者的生存率无明显差别。
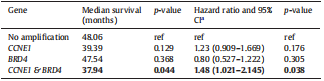
图1. CCNE1、BRD4基因扩增时中位生存期及差异表现
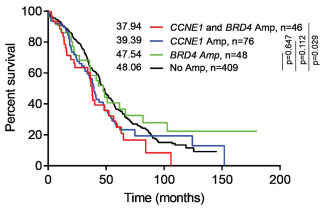
图2.CCNE1、BRD4扩增时生存曲线图
在来源于VUMC TROC TMA的110例HGSOC患者中,32例(29%)患者cyclin E和BRD4蛋白同时高表达,但是它们同时高表达并不与不良预后有关(HR=1.29),这可能与样本数少有关。Cyclin E的高表达与不良预后有关(HR=1.62),BRD4的表达与预后无关(HR=0.99)。
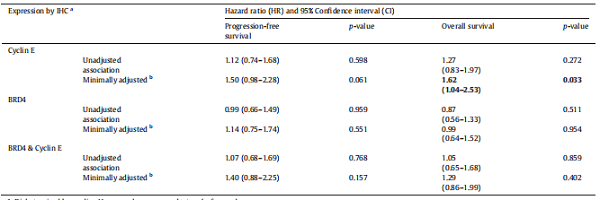
图3.HGSOC患者Cyclin E和BRD4蛋白表达与无进展生存、总生存期关系
研究得出结论:在HGSOC患者中,CCNE1和BRD4共同扩增可能与不良预后的相关性更大。另外考虑到接近30%的较高扩增比例,这有可能成为将来铂耐药的HGSOC和BRCA野生型同源重组HGSOC患者治疗的新方向。
参考文献:
Shariska Petersen, Andrew J Wilson, Jeff Hirst et al.CCNE1 and BRD4 co-amplification in high-grade serous ovarian cancer is associated with poor clinical outcomes.https://doi.org/10.1016/j.ygyno.2020.01.0380

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
