卵巢癌是女性生殖系统肿瘤中死亡率最高的瘤种,即使经过手术化疗等综合治疗,仍有70%的患者出现复发。细胞毒药物是复发性卵巢癌治疗的基石,经过强烈的化疗,仍有一部分患者面临着不断复发的噩梦。伴随着疾病的反复,复发间隔越来越短,患者体力及药物疗效也越来越差。
因此,如何在疾病缓解后延缓甚至预防复发,赠予患者更多的缓解时间成为打破复发噩梦的突破口,也是维持治疗的使命所在。PARP抑制剂的诞生,为卵巢癌的维持治疗带来了革命性的改变。
神奇的PARP抑制剂如何攻击肿瘤细胞?
让我们先来恶补下细胞生物学知识,DNA是双链结构,在细胞分裂过程中,DNA的复制会出现单链或双链的断裂。幸好人体有着极其智慧及复杂的修复系统,正常情况下,PARP,即聚腺苷二磷酸核糖聚合酶会及时地修复断裂的单链;而BRCA蛋白则负责修复双链,二者联合维护DNA双链的稳定。在PARP抑制剂的作用下,DNA单链修复功能受损。在正常细胞中,BRCA蛋白仍可发挥修复作用;而存在BRCA突变缺陷的肿瘤细胞,DNA单双链修复均失效,DNA损伤的累积导致肿瘤细胞死亡(图1)。
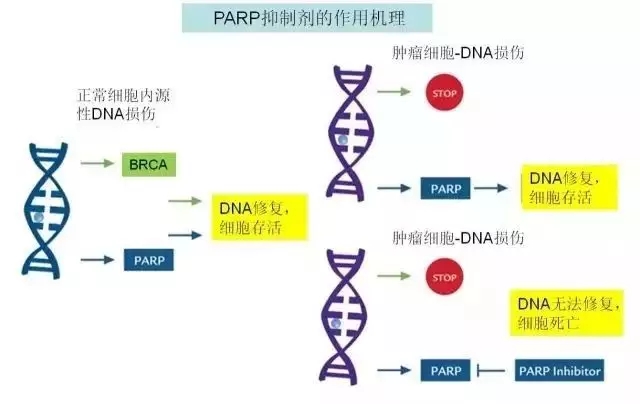
▲图1:PARP抑制剂作用机制
这么看来,PARP抑制剂似乎仅对BRCA基因突变肿瘤有效,但目前的研究证实,对于铂类敏感的肿瘤,PARP抑制剂同样能发挥强大的杀伤作用。其可能机制源于铂类药物与PARP抑制剂有着同样的作用目标——DNA双链,对铂类药物的敏感性也一定程度上反映了肿瘤细胞对PARP抑制剂的潜在敏感性。简单地说,如果肿瘤不能修复铂类导致的双链DNA的断裂,也同样不能修复PARP导致的单链DNA断裂。

有了以上的理论基础,我们隆重推出今天的主角——Niraparib(尼拉帕尼)。目前,FDA已批准上市三种PRAP抑制剂,Olaparib、Rucaparib、Niraparib用于对铂类敏感复发的二线治疗后的维持治疗。作为PARP抑制剂家族中的晚辈(第三个批准上市),Niraparib战绩傲人。它是美国FDA批准的首个无需BRCA突变或其他生物标志物检测就可用于治疗的PARP抑制剂,其没有BRCA变异限制,适用人群更为广泛。他与老大哥“Olaparib“相比,特点在哪里? 。
特点一:无论BRCA突变状态,“一视同仁”
让我们回顾一下让Niraparib获得卵巢癌维持治疗适应证的NOVA研究[1]。这是一项随机、双盲、安慰剂对照的III期临床试验,该研究入组对铂类化疗药敏感的复发性卵巢上皮癌、输卵管癌或原发性腹膜癌,且至少接受2次含铂化疗药达到CR或PR,主要终点为独立中心评审的PFS。
结果显示无论gBRCA是否突变,是否存在同源修复重组缺陷(HRD),Niraparib组的PFS均显著获益:gBRCA突变组:21个月对比5.5个月;非gBRCA突变HRD(+)组:12.9个月对比3.8个月;非gBRCA突变组:9.3个月对比3.9个月(图2)。
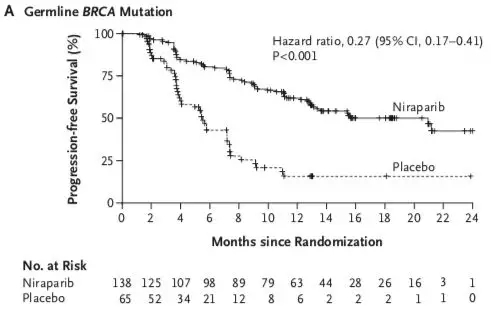
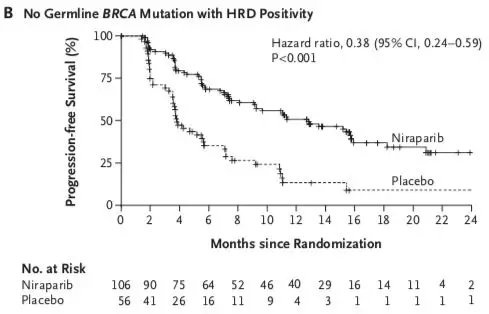
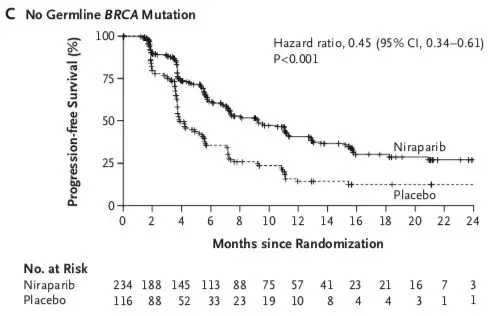
▲图2:NOVA研究不同亚组PFS时间
再看老大哥“Olaparib“,其III期临床研究SOLO2,仅入组了BRCA突变的患者;仅在II期临床研究Study19中看到BRCA野生型患者PFS的获益,因此其对BRCA野生型卵巢癌的证据级别不如Niraparib来的高。
从理论的角度分析,Niraparib发挥强大而广泛的肿瘤杀伤作用可能与其药物代谢和药代动力学特性不同有关[2]。其在肝脏中通过羧酸酯酶催化的酰胺水解途径代谢(carboxylesterase-catalysed amide hydrolysis),区别于Olaparib的细胞色素P450途径。因而其药物及食物的干扰小。
此外,Niraparib的半衰期更长(36h),生物利用度高(73%),药代动力学呈线性,使其在肿瘤组织中的暴露时间更长,浓度更高。而半衰期长也带来了Niraparib的另一项优点,只需每天服药一次,应用方便,患者依从性高。
因此,Niraparib较Olaparib兼顾了所有铂类敏感的卵巢癌患者,证据级别更高,可谓“一视同仁”。
特点二:起始剂量不能“一概而论”
骄人的战绩也伴随着不可忽略的“牺牲”,不良反应和药物相生相伴,Niraparib三期安全数据显示,以300mg为起始剂量,其总体的副反应较Olaparib大。血液性毒性是Niraparib较常见的导致减量的毒性反应。 3/4级贫血、血小板减少、中性粒细胞减少发生率分别为25.3%、33.8%及19.6%。好在因副反应治疗中断的发生比率为9.3%,与Olaparib的10.8%相近。而因副反应减量的比例达到68.9%。
这么高的减量比例是否会影响疗效?针对NOVA研究进行的RADAR分析(Rapid Adjustment of Dose to reduce Adverse Reactions)发现,基线血小板计数及基础体重与增加的≥3级的血小板减少有关,减量到200 mg或100 mg的患者,PFS和保持300 mg的患者基本一致。因此该项研究建议对于基线体重<77 kg或基线血小板计数<150000 μL的患者,在治疗初即可个性化选择起始剂量为200mg[3]。
如果说RADAR的回顾性分析数据证据级别不够,那么接下来的数据夯实了200mg起始剂量的安全性及有效性。2018年ESMO大会上公布的以200mg起始剂量接受Niraparib治疗的真实世界研究[4],共入组153例患者,结果显示,其各级别不良反应发生率均显著低于NORA研究, 3/4血小板减少率减少到2%,因不良反应中断药物治疗发生率2%,药物减量发生率11%。
PRIMA研究是尼拉帕尼在卵巢癌一线维持治疗的全球III期临床试验,中期安全数据分析基于患者体重和血小板计数结果决定尼拉帕尼给药起始剂量时,≥3级的治疗相关不良事件发生率只有17.8%。起始剂量200mg 组PFS与300mg无差异[5]
因此,为了让患者在获得疗效的同时,可以更有质量地生存,Niraparib的起始剂量不能“一概而论”。而根据患者体重及血小板计数个体化调节起始剂量,其安全性及疗效已获得回顾性,前瞻性及真实世界研究三大循证医学证据的支持。大部分中国患者体重小于77kg,完全可以考虑选择200mg作为起始剂量。
另一方面,Niraparib带来的不良反应也并没有想象中可怕,在经过规范地调整剂量,积极地对症治疗后,大部分患者还是可以获得很好的生活质量。
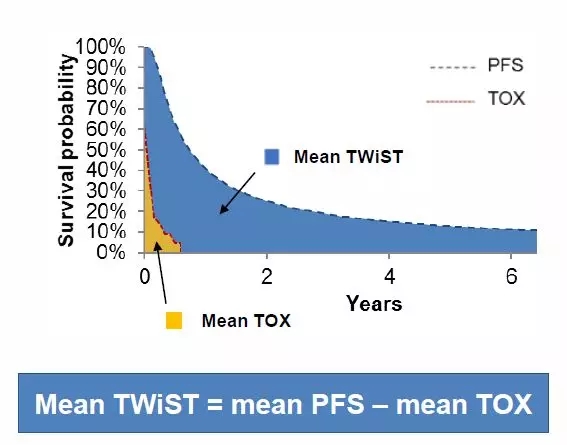
▲图3:TWiST计算方式
2019年美国妇科肿瘤学会(SGO)年会上公布的TWiST(time without symptoms or toxicity ,TWiST)分析很好地证实了这一点[6]。TWiST关注的是患者无进展生存时间与受药物不良反应影响时间的差值(图3),其结果显示与安慰剂相比,接受尼拉帕尼治疗的患者平均TWiST增加,即获得了更多高生存质量的PFS(图4)。
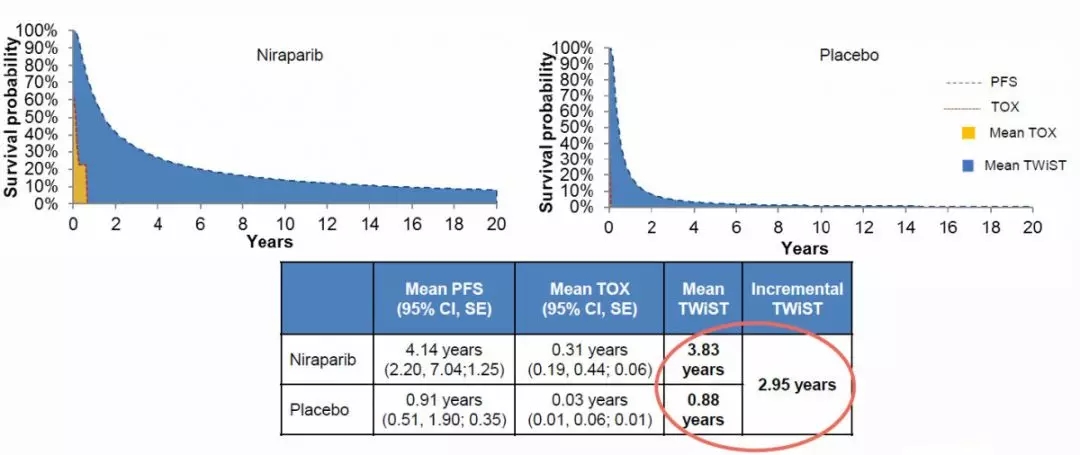
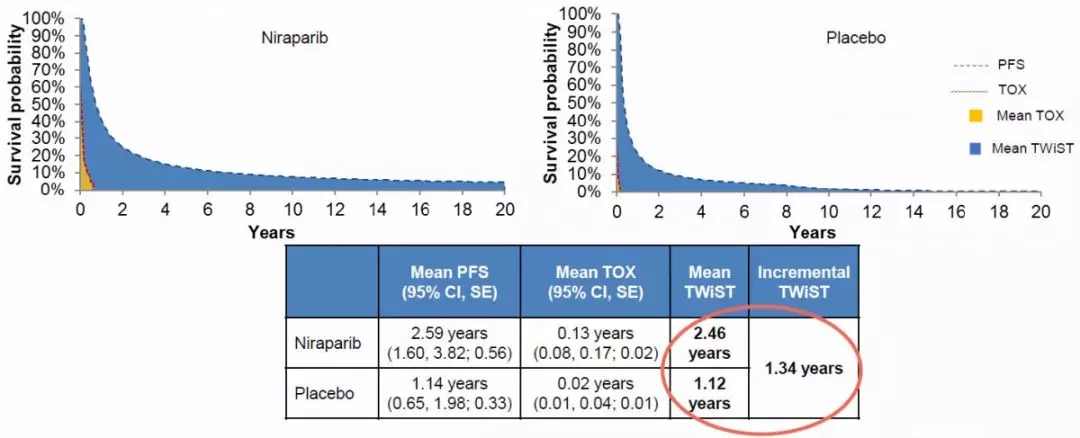
▲图4:gBRCA突变队列(上)及gBRCA未突变队列(下)TWiST结果
综上,复发性卵巢癌的噩梦需要新的治疗方式来打破,Niraparib为铂类敏感复发的二线治疗后的维持治疗阵营再添一将,其对是否存在BRCA突变“一视同仁”,疗效卓越;但为获得更好的安全性,起始剂量不能“一概而论”,需根据患者特征根据循证医学证据个性化选择。经过合理的调节剂量,积极管理不良反应,患者可以获得高质量的生存获益。
2018年12月12日,尼拉帕尼内地新药上市申请已经获国家药品监督管理局受理,我们期盼其早日上市,让中国卵巢癌患者获得更多高质量的生存时间。
参考文献:
[1] Mirza M R, Monk B J, Herrstedt J, et al. Niraparib maintenance therapy in platinum-sensitive, recurrent ovarian cancer[J]. New England Journal of Medicine, 2016, 375(22): 2154-2164.
[2] LaFargue C J, Dal Molin G Z, Sood A K, et al. Exploring and comparing adverse events between PARP inhibitors[J]. The Lancet Oncology, 2019, 20(1): e15-e28.
[3] Berek JS, Matulonis UA, Peen U, et al. Safety and dose modifcation for patients receiving niraparib. Ann Oncol 2018; published online Aug 1. DOI:10.1093/annonc/mdy181.
[4]Jack R. Gallagher, et al. Real world occurrence of top three clinical-trial reported adverse events of PARP inhibitor niraparib maintenance therapy in platinum-sensitive, recurrent ovarian cancer, a national retrospective observational study of a 200?mg/day starting-dose cohort. Annals of Oncology, 2018, 29(suppl_8)
[5] Gonzalez A, Mirza M R, Vergote I, et al. 941PD A prospective evaluation of tolerability of niraparib dosing based upon baseline body weight (wt) and platelet (blplt) count: Blinded pooled interim safety data from the PRIMA Study[J]. Annals of Oncology, 2018, 29(suppl_8): mdy285. 150.
[6]Matulonis UA, Walder L, N?ttrup TJ, et al. Time without symptoms or toxicity in patients with recurrent ovarian cancer receiving niraparib maintenance treatment versus placebo: A TWIST analysis of the ENGOT-OV16/NOVA trial. Presented at: 2019 SGO Annual Meeting. March 16-19, 2019; Honolulu, HI. Abstract 1.

扫二维码
关注OC资讯
