近年来,PARP抑制剂(PARPi)的问世极大地改变了卵巢癌的治疗格局,也被尝试用于既往接受过≥2线化疗的BRCA突变的铂耐药卵巢癌患者,PARP抑制剂联合抗血管生成抑制剂能否成为铂耐药复发卵巢癌患者更优的治疗选择?
中山大学肿瘤防治中心妇科刘继红教授领导的团队在柳叶刀子刊eClinicalMedicine在线发表了题为“尼拉帕利联合安罗替尼用于铂耐药复发性卵巢癌治疗的疗效与安全性研究(ANNIE研究)”的文章。该研究发现,尼拉帕利联合安罗替尼组合疗法在铂耐药复发卵巢癌患者中显示出良好的抗肿瘤活性和可耐受的毒性,这可能为该类肿瘤患者提供一种潜在的新治疗选择。本期OC文献精读特邀该研究的subi刘国臣教授解密安尼研究背后的故事。

 00:000:00 音频
00:000:00 音频

研究的临床意义
1-本研究之前的证据
PARP抑制剂和抗血管生成药物联合方案是铂耐药复发性卵巢癌的一个潜在“去化疗”组合。本研究之前,通过关键词(“PARP抑制剂”)和(“抗血管生成药物”)和(“铂耐药卵巢癌”)检索了截至2022年2月发表在PubMed和Web of Science的相关文献,是唯一的此类组合,然而,西地尼布+奥拉帕利组合的疗效和安全性并不令人满意,但是尼拉帕利和安罗替尼具有不同的代谢途径,药物相互作用极小,有利于该组合安全有效的发挥抗肿瘤活性。
2-本研究的附加价值
ANNIE是研究尼拉帕利和安罗替尼联合治疗铂耐药卵巢癌的首项研究。本研究的疗效数据和安全性特征表明,尼拉帕利在铂耐药疾病中具有有利的风险-获益特征。ANNIE研究提供了该组合可能改善铂耐药卵巢癌患者客观缓解率和无进展生存期的初步证据。
研究背景
1-铂耐药患者的治疗选择有限
上皮性卵巢癌由于缺乏有效的筛查方法,超过70%的患者初诊即为晚期。尽管铂类和紫杉烷类化疗最初会产生缓解,但大多数患者2年内会复发,随着复发间期的逐渐缩短,这些患者最终将从铂敏感复发进展为铂耐药复发。对于铂耐药卵巢癌患者,有效的治疗选择有限。标准非铂类化疗的客观缓解率 (ORR)为10%-30%,无进展生存期(PFS)为2-5个月。抗血管生成药物贝伐珠单抗与化疗联合使用时显著改善了PFS和ORR,但不良事件的发生率也明显增加。此外,许多铂耐药患者既往接受过多线化疗,健康状况受损,无法耐受进一步的足剂量或频率的化疗,需要耐受性更好的治疗方案。而贝伐珠单抗静脉给药和大多数化疗也会给患者带来不便,并可能影响生活质量。
2-PARPi+抗VEGFi组合在铂耐药的探索与协同机制
抗血管生成药物和PARP抑制剂均在卵巢癌治疗中发挥重要作用,且二者联合治疗作为新型治疗选择的研究越来越多。临床前研究表明,抗血管生成药物可通过微环境缺氧和同源重组修复下调来诱导HRD。相反,PARP1可能参与血管生成,因此PARP抑制剂也可能带来额外的抗血管生成作用。这是两者之间潜在协同作用机制的基础,此后在铂敏感复发性卵巢癌中证明了西地尼布+奥拉帕利和尼拉帕利-贝伐珠单抗联合治疗的协同作用。PARP抑制剂和靶向血管内皮生长因子 (VEGF) 和 VEGF 受体 (VEGFR) 信号通路的抗血管生成药物均已在铂耐药和/或复发性卵巢癌中显示出抗肿瘤活性。研究这两类药物联合治疗是否会提高铂耐药卵巢癌的疗效是有意义的,其中西地尼布-奥拉帕利是迄今为止唯一广泛评价的联合治疗。中国的一些医疗机构曾在多线化疗失败且无任何其他治疗选择的铂耐药卵巢癌患者中观察到尼拉帕利联合安罗替尼不错的临床疗效(经充分知情同意),提供了临床前证据,表明尼拉帕利+安罗替尼联合治疗可能是该人群值得探索的一种新的治疗选择。
尼拉帕利是一种高选择性 PARP1/2 抑制剂,获批用于新诊断或铂敏感的复发性卵巢癌的维持治疗。即使是在HRD阴性晚期卵巢癌患者中,尼拉帕利也有临床获益。在 AVANOVA 研究中,尼拉帕利和贝伐珠单抗联合治疗在铂敏感的复发性卵巢癌患者中,疗效优于尼拉帕利单药治疗,且不良反应可耐受。
安罗替尼是一种口服小分子受体酪氨酸激酶抑制剂 (TKI),靶向VEGFR1/2/3、c-Kit、PDGFR-α和成纤维细胞生长因子受体 (FGFR1/2/3),对肿瘤血管生成和生长具有广谱抑制作用。安罗替尼在中国获批用于多种癌症的挽救治疗,包括肺癌和软组织肉瘤。越来越多的证据表明安罗替尼在铂耐药卵巢癌也有一定疗效。尼拉帕利和安罗替尼具有不同的代谢途径,因此药物间相互作用极小,有利于这些药物联合安全使用。在本研究中,我们评估了尼拉帕利和安罗替尼联合治疗铂耐药卵巢癌患者的安全性和活性。
研究设计
ANNIE研究共入组40例患者,关键入组标准:年龄为18-70岁,经组织学确认为卵巢上皮癌、输卵管癌或原发性腹膜癌,在含铂化疗末次给药后6个月内复发,经实体瘤疗效评价标准 (RECIST1.1)评估有可测量的病灶,患者的预期寿命必须超过16周,ECOG评分为0或1。患者口服尼拉帕利胶囊300mg/200mg(根据基线体重:≥77Kg,300mg;<77Kg,200mg),每日一次,连续给药,口服安罗替尼12 mg(2020年11月01日起,初始剂量减至10mg),连续服药2周,停药1周,每21天为一个周期,直至疾病进展或出现不可耐受的毒性。随访期间要求患者在随访手册中记录每日用药、心率、血压和症状,研究工作人员每周电话联系所有患者,患者在出现异常症状时立即联系研究工作人员。每3周进行一次血液学和血清生化检查、尿液检查和心电图检查(前4周每周进行一次全血细胞计数)。在基线和之后每3个周期一次使用计算机断层扫描或磁共振成像进行肿瘤评估。由中心放射学委员会根据RECIST 1.1标准评估肿瘤进展,并由未参与研究的两名外部的独立放射科专家审查以进行敏感性评估。完全或部分缓解必须在首次记录缓解后>4周确认。单独CA125升高不视为疾病进展。治疗中止后,记录研究药物末次给药后30天内的不良事件,每90天随访一次患者的生存期和后续抗肿瘤治疗。
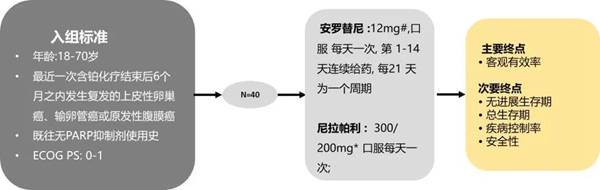
研究终点
■ 主要终点为RECIST1.1评估的ORR(确认完全或部分缓解的患者百分比)。
■ 次要疗效终点包括PFS、至缓解时间 (TTR)、缓解持续时间 (DOR)、无铂治疗间期 (PFI) 和总生存期 (OS)。
■ 安全性终点包括治疗期间出现的不良事件 (TEAE) 的发生率、严重程度和药物相关性。
统计学分析
既往化疗单药治疗铂耐药卵巢癌的缓解率约为20%。假设尼拉帕利联合安罗替尼的真实ORR为40%,则估计36例患者的样本量可提供80%的把握度以拒绝ORR≤20%的无效假设,单侧 I 类错误率为5%,假设失访率为10%,计划的目标样本量为40例患者。计划在入组结束后第24周进行中期分析,如果 ORR低于20%,将终止研究。计算意向治疗(ITT)人群(接受至少一剂研究药物的所有患者)和疗效可评价人群(可获得至少一次基线后肿瘤评估结果的患者)的ORR。使用 Clopper-Pearson 方法计算 ORR 的点估计值和双侧95%CI。对于至事件时间终点,使用Kaplan–Meier法估计中位数和相应的双侧95%CI。对于事后亚组分析,使用将分层因素作为协变量的 Cox 模型估计HR和相应的95%CI。在 ITT 人群中分析安全性结果,并按患者例数和百分比汇总。使用SAS(SAS Institute)9.4版进行统计分析。
研究结果
1-基线人口统计学和临床特征
2020年05月22日至2021年04月22日期间,3家研究中心共入组40例患者,全部接受尼拉帕利和安罗替尼治疗。仅1例体重78kg的患者接受尼拉帕利300 mg的起始剂量。数据分析截止日期为2022年01月31日,随访正在进行中。中位随访时间为15.4个月 (95%CI 12.6-17.7),4例患者仍在接受治疗。中止治疗的原因为疾病进展 (n = 24)、不良事件 (n = 5)、患者要求 (n = 6) 和方案违背(n = 1,接受化疗)。基线特征见表1。
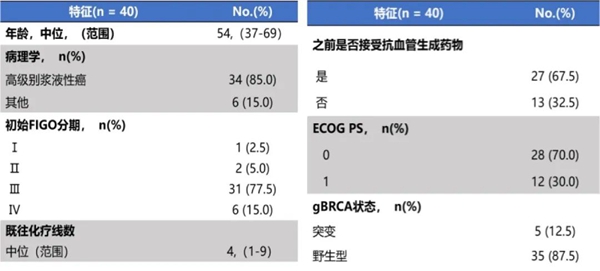
2-疗效结果
截至数据截止日期,ITT人群的ORR为50.0%(95%CI 33.8-66.2),包括1例完全缓解和19例部分缓解(表2)。4例患者退出研究时未进行基线后肿瘤评估,剩余36例患者组成了疗效可评价人群,ORR为55.6%(95%CI 38.1-72.1)。对于基线gBRCAmut患者,ORR为100%(95%CI 47.8-100,5/5),而gBRCA野生型患者的ORR为42.9%(95%CI 26.3-60.6;15/35)。30例高级别浆液性腺癌患者的ORR为50.0%,中位TTR、DOR和PFI分别为2.8个月(95%CI:1.6-4.9)和6.9个月(95%CI 4.2–9.7)和13.2个月(95%CI 11.0–17.7)。24例患者发生PFS事件(均为疾病进展),中位 PFS为9.2个月(95%CI 7.4–11.9),17例患者死亡,中位 OS 为15.3个月(95%CI 13.9-不可评价)(3B)。既往使用抗血管生成药物不影响PFS,既往抗血管生成药物的使用和化疗的线数不影响OS。
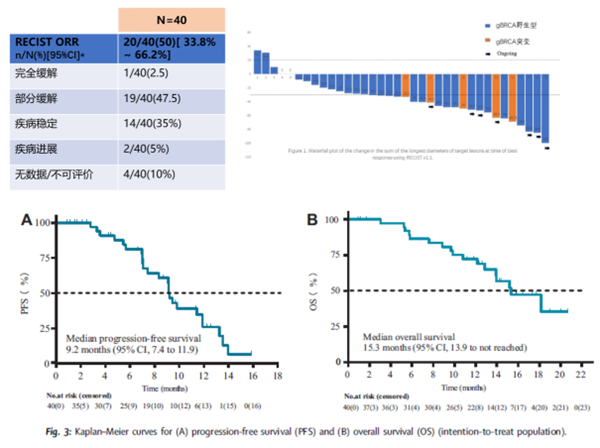
表2
3-安全性
最常见的任何级别TEAE(表3)为高血压(22例患者,55%)、白细胞减少症(18例患者,45%)和手足综合征(17例患者,43%)。26例患者 (68%) 报告药物相关的≥3级TEAE,未记录到治疗相关死亡或骨髓增生异常综合征。安罗替尼组和尼拉帕利组分别有21例患者和19例患者因TEAE而剂量下调,11例患者两种药物均发生剂量下调。安罗替尼组和尼拉帕利组分别有14例患者和21例患者因TEAE而给药中断,4例患者因TEAE中止治疗,其中2例停用两种药物,各有1例患者仅停用尼拉帕利或安罗替尼。
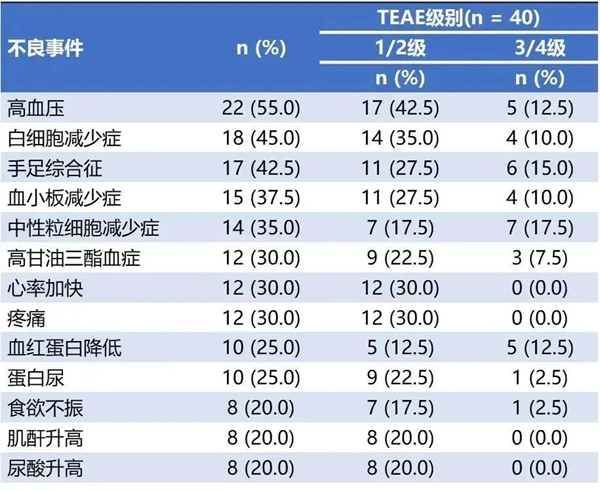
表3
研究设计
1-安尼组合突破biomarker和既往贝伐使用史的限制
本研究表明,尼拉帕利-安罗替尼联合治疗可能为目前治疗选择非常有限的铂耐药卵巢癌患者提供一种潜在的新型治疗方案,联合治疗的耐受性也良好,与单药相比,未观察到新的安全性信号。由于贝伐珠单抗被广泛推荐用于晚期或复发性卵巢癌,本研究中的大多数患者既往接受过抗血管生成治疗,结果表明,抗血管生成药物的治疗史似乎不影响后续应用安罗替尼联合尼拉帕利的疗效。另一种已在铂耐药卵巢癌中评价的血管生成联合PARP抑制剂的组合是西地尼布加奥拉帕利,在4项 II 期研究 (NCT02345265、CONCERTO、BAROCCO、OCTOVA) 中,观察到西地尼布-奥拉帕利在携带或不携带gBRCAmut的患者中可达到15%-20%的ORR;中位PFS 5.1–5.6个月在数值上长于紫杉醇每周一次给药(3.1–3.9个月),但尚未确定统计学优效性。在我们的研究中,患者组的ORR为50%,其中仅13%(5/40) 的患者携带gBRCAmut,结果令人鼓舞,表明尼拉帕利联合安罗替尼可以克服PARP抑制剂单药治疗的生物标志物限制,使更广泛的铂耐药患者人群获益。同样值得注意的是,我们研究中的中位PFS超过半年,且可转化为相当长的PFI。我们的一些患者在研究治疗结束后对进一步的含铂化疗有客观应答,这是一个有趣的观察结果,需要进一步研究来验证。
2-安尼组合的毒性与单药相比,AE发生率并未增加
在我们的研究中,未观察到尼拉帕利+安罗替尼的新安全性信号,与相应的单药安全性特征相比。血液学毒性(尤其是贫血)的发生频率低于其他尼拉帕利单药的临床试验。这可能与安罗替尼造成的低氧环境有关,有研究表明缺氧诱导因子通过调节促红细胞生成素的表达来促进红细胞生成。与早期使用固定起始剂量300mg进行的尼拉帕利研究不同,我们的研究使用了基于体重的个体化起始剂量,其中大多数患者的尼拉帕利起始剂量为200 mg。此外,通过严格的常规血液检查,一旦患者的血小板水平降至100 000/μL以下,立即停用研究药物。这些指标可能导致观察到的3–4级血小板减少症发生率降低。与既往研究相比,与安罗替尼相关的常见不良事件,如高血压、手足综合征和某些生化异常的发生率未增加。关于安罗替尼起始剂量降低的方案修正案(参见程序),尽管在入组的前23例接受12 mg安罗替尼治疗的患者中观察到TEAE(主要是手足综合征和高血压)的发生率相对较高,但TEAE大多为1-2级,可通过方案规定的剂量调整进行管理。本研究中3-4级TEAE 主要为中性粒细胞减少症、手足综合征、高血压和贫血,可管理和控制。值得注意的是,晚期患者往往骨髓功能较差,因此更容易发生≥3级骨髓抑制相关TEAE。我们计划在未来研究中通过可能的剂量选择进一步探索TEAE 的预防和管理。
3-尼拉帕利独特代谢途径,使两药都可按常用临床剂量给药,有利于优化疗效
大多数小分子TKI(如安罗替尼、西地尼布、帕唑帕尼和阿帕替尼)通过CYP450途径代谢,大多数PARP抑制剂(如奥拉帕利、芦卡帕利、帕米帕利和氟唑帕利)也是如此。因此,抗血管生成药物和PARP抑制剂联合给药的最大耐受剂量通常低于单药的常用临床剂量。在西地尼布-奥拉帕利研究中,西地尼布(20mgQD而不是30mgQD)或奥拉帕利(200 mg BID而不是300mg BID)需要降低剂量水平;通过间歇性给药进一步降低剂量可改善安全性,但却以牺牲PFS为代价。相反,尼拉帕利可被羧酸酯酶代谢,与经CYP450途径代谢的药物发生药物间相互作用的可能性极低。在我们的研究中,尼拉帕利和安罗替尼均以常用临床剂量给药,且耐受性良好。使用临床足剂量有利于优化疗效,还允许在必要时有更大的剂量调整空间来管理TEAE并改善患者的生活质量。
4-局限性
本研究也存在一些局限性。首先,这是一项单组、II期研究,样本量较小。尽管我们观察到ORR增加和PFS延长趋势,但需要在大样本试验中验证长期疗效。其次,无法确定HRD状态与疗效之间的关系,因为难以从既往接受过大量治疗的患者人群中获得有效标本。第三,本研究排除了既往暴露于PARP抑制剂的患者,考虑到PARP抑制剂在卵巢癌中的广泛一线应用,这些患者可能占铂耐药卵巢癌患者的相当大比例。我们计划进行一项扩展研究(ANNIE Plus),纳入既往接受过PARP抑制剂治疗的患者,以加强我们研究结果的临床相关性。第四,COVID-19大流行排除了对一些患者进行定期现场随访。我们进行了密切的电话随访,通过邮寄方式提供研究药物,并在可能的情况下将患者引导到当地医院,以尽量减少现场随访减少的影响。
总之,尼拉帕利和安罗替尼的联合治疗在铂耐药卵巢癌患者中显示出良好的抗肿瘤活性和可耐受的毒性。这种口服、去化疗的联合治疗可能代表铂耐药卵巢癌患者一种潜在的新治疗选择。
参考文献:
1. EClinicalMedicine. 2022 Nov 30;54:101767. doi: 10.1016/j.eclinm.2022.101767.

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
