晚期上皮性卵巢癌患者铂耐药预示预后不良。通过不同机制抑制血管内皮生长,可能获得更持久的抗血管生成疗效从而改善患者生存。今天我们请到金华市中心医院张琳医生来解读2022年8月发表在《Journal of Clinical Oncology》上的文章《那赛昔珠单抗联合紫杉醇治疗铂耐药卵巢癌的 Ib 期研究》。那赛昔珠单抗(navicixizumab)是一种首创的双特异性抗血管生成抗体,靶向DLL4和VEGF,从而诱导抗肿瘤反应,同时有抗血管生成的作用。


 00:000:00 音频
00:000:00 音频
01 研究设计
■ 开放标签、非随机、剂量递增的Ib期试验
■ 主要终点:那赛昔珠单抗的最大耐受剂量
■ 次要终点:安全性、免疫原性、ORR、PFS等
基于 RNA 表达的新型生物标志物回顾性检验了以下假设:肿瘤微环境TME亚型可作为常规性免疫治疗生物标志物,免疫激活TME为生物标志物阳性,免疫抑制TMEs为生物标志物阴性,前者更可能对那赛昔珠单抗产生应答。
■ 本研究共纳入44例患者
● 43例(97.7%)曾接受过紫杉醇治疗
● 30例(68.2%)接受过贝伐珠单抗治疗
● 20例(45.5%)接受过PARP抑制剂治疗
● 39例患者被纳入扩展队列,并以3 mg/kg的剂量进行治疗
02 研究结果
1 安全性
● 入组患者接受那赛昔珠单抗剂量为 3 mg/kg 每2周一次。
● 未发生剂量限制性毒性。
● 患者接受了中位8次那赛昔珠单抗给药,中位给药时间为113天。
● 最常见的3/4级治疗相关不良事件为高血压 (40.9%)、中性粒细胞减少 (6.8%) 和血小板减少 (4.5%)。18.2%的患者发生肺动脉高压(1-2级)。未发生5级治疗相关的不良事件。
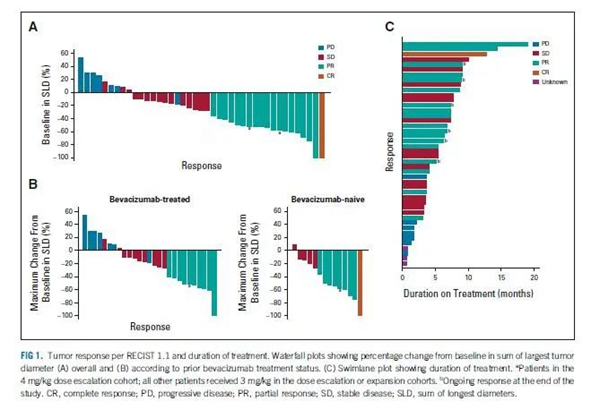
2 临床疗效
● 总体客观缓解率为43.2%:既往接受贝伐珠单抗治疗的患者为33.3%,未经贝伐珠单抗治疗的患者为64.3%,生物标志物阳性患者为62%。
● 疾病控制率 (DCR) 为77.3%。
● 总体人群的中位 PFS 为7.2个月,贝伐珠单抗经治患者为5.4个月和贝伐珠单抗未治患者7.6个月。
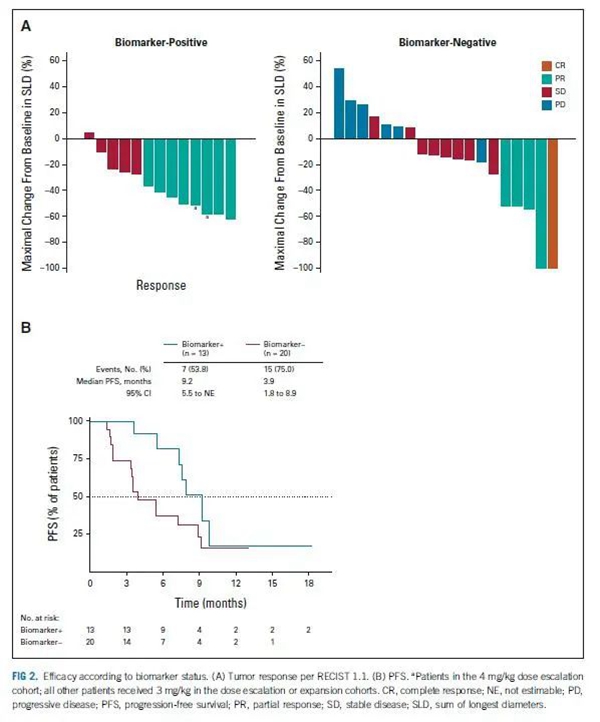
3 生物标志物
● 在生物标志物阳性患者中,ORR为62%,DCR为100%。
● 而生物标志物阴性患者中分别为25%和65%,观察到最佳缓解仅为PD。
● 与生物标志物阴性组相比,生物标志物阳性组的中位 PFS 延长5.3个月(9.2 vs 3.9个月,风险比0.43[95%CI,0.188-0.999])。
因此,研究提示具有血管生成或免疫抑制的肿瘤微环境亚型的肿瘤(生物标志物阳性)比免疫活性/沙漠化的肿瘤微环境亚型(生物标志物阴性)更有可能对那赛昔珠单抗产生反应。
专家点评
铂耐药卵巢癌患者的有效治疗手段有限,以非铂化疗为主,是目前临床上迫切需要解决的问题。研究表明,那赛昔珠单抗联合紫杉醇在铂耐药卵巢癌患者人群中具有良好的临床活性和可管理的安全性。但是仍需要一项随机研究来比较那赛昔珠单抗单药治疗或与紫杉醇联合治疗的疗效,并确定是否可以使用该生物标志物来预测更可能从那赛昔珠单抗获益的患者。

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
