本期OC文献精读邀请到了河南省肿瘤医院-妇瘤科-刘若男教授解读于2014年4月发表在Journal of clinical oncology的一篇题为《贝伐珠单抗在晚期卵巢癌一线治疗III期随机试验中胃肠道不良事件的风险因素:一项GOG的研究(GOG218)》的文章。


 00:000:00 音频
00:000:00 音频
一、研究背景
将贝伐珠单抗纳入卵巢癌一线治疗一直存在着争议,因为既往的两项一线III 期试验中,整体研究人群均缺乏总生存的获益,并且有产生额外毒性风险的可能性。胃肠道壁破裂可能是最令人担忧的与贝伐珠单抗相关的不良反应,报告率约为2.4%。这种并发症的发病机制尚不清楚,特定的风险因素仅在历史研究中被提及。因此,妇科肿瘤小组(GOG)在GOG218这项前瞻性一线III期临床试验中,(预先设计)评估贝伐珠单抗用于一线卵巢癌治疗中出现胃肠道不良事件(AEs)的风险因素,探索其胃肠道安全性。据了解,这也是第一项抗VEGF药物治疗实体瘤背景下检验严重 GI AE 风险因素的前瞻性研究。
二、研究设计
如图1所示,GOG 0218是一项双盲、安慰剂对照的一线III期临床试验。1873例晚期癌症患者被随机分配到三个术后治疗方案中:
R1(无贝伐珠单抗组):6个周期静脉卡铂-紫杉醇化疗+安慰剂周期(C,cycle) C2-C22;
R2(贝伐珠单抗治疗组):6个周期静脉卡铂-紫杉醇化疗+贝伐珠单抗(15mg/kg /3week)C2-C6+安慰剂C7-C22;
R3(贝伐珠单抗治疗+维持组):6个周期静脉卡铂-紫杉醇化疗+贝伐珠单抗(15mg/kg /3week)C2-C22。
评估患者潜在风险因素的历史或研究进展,GI AEs的定义为2级穿孔、瘘、坏死或出血。
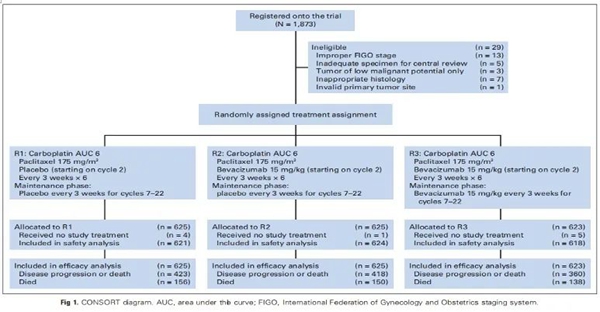
图1.研究设计
三、研究结果
1、基线特征(表1、表2)
■ 入组GOG 0218的1873例患者的基线特征在治疗组间分布相似(表1)。中位年龄为60岁;超过80%的患者患有浆液性腺癌;大多数肿瘤分级为3级;40%为III期患者;在PDS术后腹腔内残留病灶直径>1cm;26%的患者为IV 期。
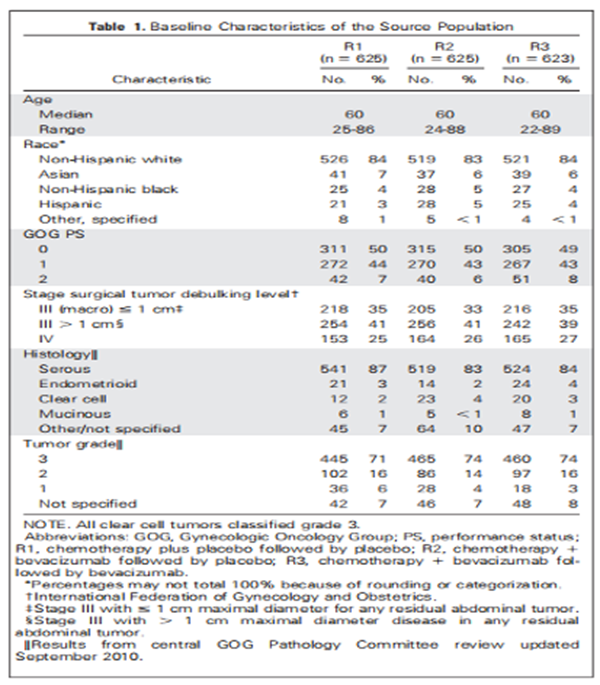
■ 收集了入组的1873例患者中1759例 (94%) 的病史(MEDH)(表2)。如表2所示,假定的GI AEs医学风险因素在三个治疗组中的分布频率类似。值得注意的是,至少30%的患者有血管危险因素,582例 (33%) 正在接受高血压药物治疗,226例 (12.8%) 在过去一年内吸烟。关于胃肠道疾病,在卵巢癌PDS术时147例患者 (8.3%) 接受小肠切除术(SBR) ,306例 (17.4%)接受了大肠切除术 (LBR)。
■ 入组患者在治疗期间潜在风险因素的进展比率较低,包括39例 (2.2%)胃肠道梗阻患者、86例 (4.9%) 复杂性中性粒细胞减少症(发热或4级)患者和100例 (5.7%) 合并动脉或静脉血栓栓塞事件患者。
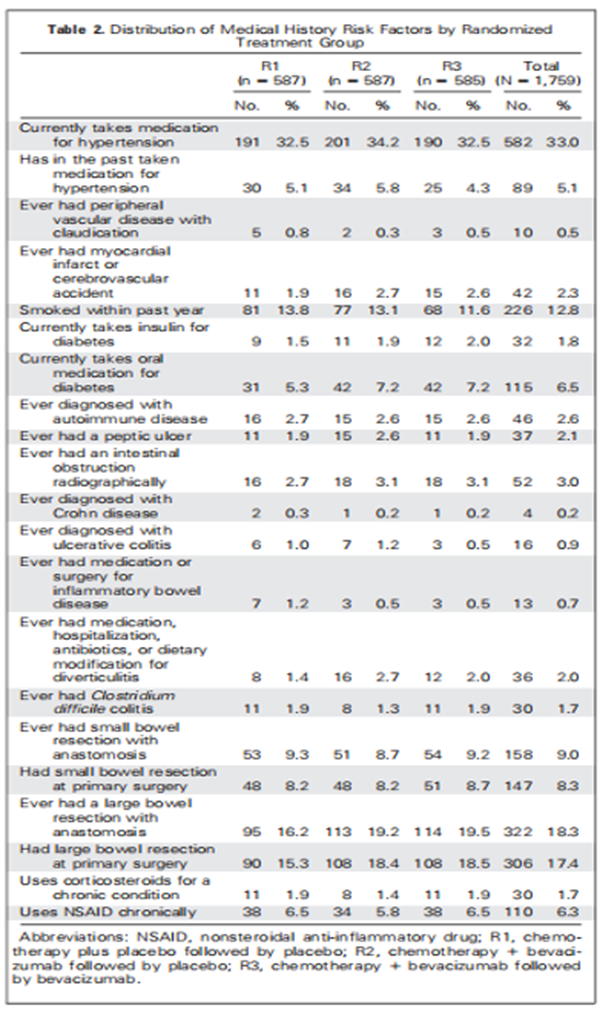
2、胃肠道AEs的发生率和类型(表3、图2)
总体而言,57例患者 (3.2%) 发生GI AE,其中50例患者 (2.8%) 的AE发生在C2(开始贝伐珠单抗或安慰剂治疗)治疗期间或之后。R1、R2和R3组分别有1.7% (10/587例)、3.4% (20/587例) 和3.4% (20/585例) 的患者GI AE报告,3例患者(1例3级出血患者、1例3级瘘患者和1例5级肠坏死患者)未提交MEDH病例报告表,从本报告中排除。
如表3所示,最常见的GI AE类型为穿孔20例(40%),其次是出血14例 (28%) 和瘘12例 (24%)。尽管R1治疗组中无4级或5级事件,但R2组中6例 (1%) 和R3组中4例 (0.7%) 发生了归类为危及生命或致死性的事件。
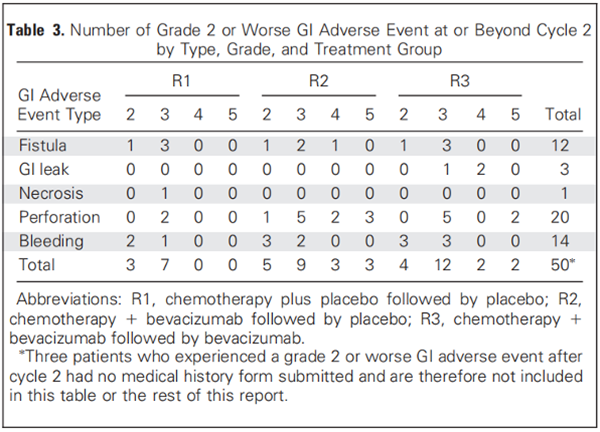
图2事件的发生时间与治疗组和周期的关系。GI AE 46例(92%)发生在C2至C6(化疗期),其中38例(75%)发生在C4。
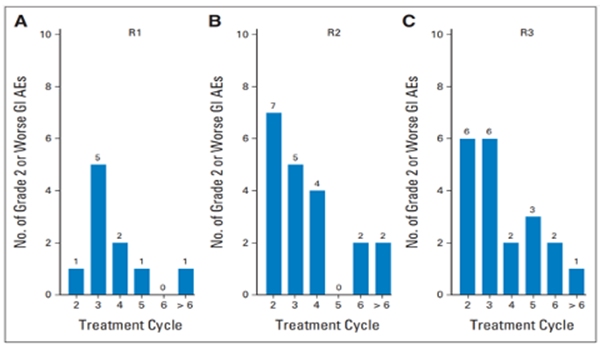
Fig 2. Number of treatment cycles before grade 2 or worse GI adverse event(AE). There were seven GI AEs before treatment cycle 2 that are not included in this figure. R1, chemotherapy plus placebo followed by placebo; R2, chemotherapy bevacizumab followed by placebo;R3, chemotherapy bevacizumab followed by bevacizumab.
3、风险因素与GI AEs 之间的相关性
■ 单变量分析表明GI AE与入组时年龄 (P=0.593)、基线PS(P=0.297)、减瘤手术后的分期和疾病残留状态 (P=0.378)、从手术到C1治疗的时间 (P=0.625) 或从手术至C2治疗的时间(P=0.997;数据未显示)无关。与研究期间发生的GI梗阻 (P=0.625)、血栓栓塞事件 (P=0.202) 或并发中性粒细胞减少症(P=0.094,仅线上)之间也无显著相关性。在时间依赖性比例风险模型中,研究人群中74名在GI AE发生前出现发热性中性粒细胞减少症的患者发生GI AE的几率更大,风险比为2.55(95%置信区间,0.607-10.74),但无统计学意义 (P=0.201)。
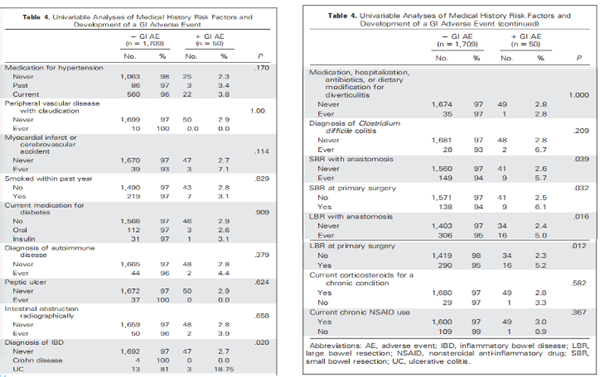
■ 如表4所示,观察到炎症性肠病 (IBD;P=0.020) 或IBD治疗史 (P=0.005);SBR吻合术 (P=0.039) 或PDS时的SBR(P=0.032);LBR吻合术 (P=0.016) 或PDS时的LBR(P=0.012) 与GI AE显著相关。使用多变量逻辑模型估算与贝伐珠单抗相关的GI AE的几率,校正了显著相关的风险因素:IBD治疗、PDS时的SBR和LBR。相对于R1,R2和R3的GI AE比值比分别为2.15(95%CI,0.981-4.71) 和2.15(95%CI,0.981-4.70)。由于每个贝伐珠单抗治疗组相对于安慰剂组发生GI AE的几率相似,因此将这两组合并为一组,以方便更精确估算贝伐珠单抗相对于安慰剂的效应。
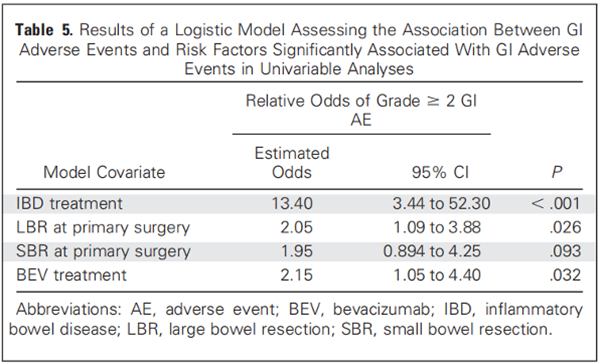
■ 如表5所示,多变量分析预估贝伐珠单抗独立增加GI AE的发生率为2.15(95%CI,1.049-4.40;精确P=0.032),这与单变量的估计值2.19相似。PDS术时IBD和LBR的既往治疗也与几率增加独立相关,而SBR对几率增加的影响程度与LBR相似,但无统计学意义(P=0.093)。
四、讨论
基于研究结果,研究者得出结论:在晚期卵巢癌的PDS术中,IBD的治疗史和结肠切除术似乎增加了铂-紫杉醇为基础的一线治疗中肠穿孔、瘘、坏死或出血的风险。
■ 在考虑了这些风险因素后,贝伐珠单抗一线治疗也增加了此类GI AE的几率,但当完成铂-紫杉醇一线化疗后继续使用贝伐珠单抗时,似乎不会与这些其他风险因素协同作用或增加GI AE的几率。
■ 对于准备手术后一线治疗的患者,应仔细告知这些干预措施和状态对其发生GI AE个体风险的潜在影响。
专家点评
■ 在本研究中,每个贝伐珠单抗治疗组的GI AE发生率为3.4%,约为单独化疗组的两倍,并且在多变量分析中,仍然是一个独立的风险因素。
■ 尽管贝伐珠单抗可能导致肠穿孔发生的机制仍不明确,但大多数数据表明 GI损伤部位的愈合受损是共同点。来自贝伐珠单抗作为转移性结直肠癌一线治疗的两项III期随机试验的汇总数据(涉及1132例患者)表明,接受贝伐珠单抗治疗的患者,手术伤口愈合并发症发生率为1.3%,而对照患者为0.5%。虽然没有结论,但是根据回顾性分析临床、病理和放射学数据提示,贝伐珠单抗诱导的肿瘤坏死可能对肠壁造成侵袭。
■ 对来自17项随机对照试验的12294例各种非妇科实体瘤患者的一项荟萃分析结果,支持贝伐珠单抗暴露与当前研究中GI AE的比值比增加(比值比为2.15)相关这一发现。这表明接受贝伐珠单抗治疗的患者中GI穿孔的发生率为0.9%,与对照患者相比,GI穿孔的相对几率为2.14(95%CI,1.19-3.85;P=0.011)。
■ 结合贝伐珠单抗已公布的研究数据,卵巢癌临床治疗中可以考虑以PARP抑制剂为代表的更优方案。

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
