PARP抑制剂联合免疫检查点抑制剂可能产生协同作用,其疗效在铂耐药复发性卵巢癌中得以证实。尼拉帕利联合帕博利珠单抗用于铂耐药复发性卵巢癌的疾病控制率达65%;尼拉帕利联合多塔利单抗和贝伐单抗的疾病控制率达76.9%。此前研究报道PARP抑制剂在胚系BRCA突变的胰腺癌维持治疗中有效,但胰腺癌BRCA突变概率仅为4%~7%。尼拉帕利在缺乏BRCA或DDR基因突变的卵巢癌维持治疗中也能取得良好疗效,实现了全人群获益。那么在胰腺癌维持治疗中,尼拉帕利联合免疫检查点抑制剂能否突破DDR基因突变的限制,使更多癌患者从维持治疗中获益呢?
本期OC文献精读特邀中山大学肿瘤防治中心王风华教授,与大家分享一篇2022年7月刊登在Lancet Oncology(IF=54.433)的文章:尼拉帕利联合纳武利尤单抗或尼拉帕利联合伊匹木单抗用于铂敏感晚期胰腺癌的Ib/II期研究。我们与王教授一起揭秘尼拉帕利联合免疫检查点抑制剂在晚期胰腺癌维持治疗的探索。


 00:000:00 音频
00:000:00 音频
一、背景
晚期胰腺癌患者采用非细胞毒性药物治疗可以避免化疗耐药和毒性累积。PARP抑制剂通过抑制和捕获PARP酶,导致DNA损伤无法修复和基因组不稳定,最终引起细胞死亡。胰腺癌合并DNA损伤修复(DNA damage repair, DDR)缺陷的患者对含铂化疗高度敏感。此前研究中,奥拉帕利(一种PARP抑制剂)对胚系BRCA1/2突变的晚期胰腺癌有效。对于没有BRCA突变的患者,能否从PARP抑制剂治疗中获益成为研究热点。
尼拉帕利是一种高选择性的PARP1/2抑制剂,对PARP酶的捕获作用更强,大约是奥拉帕利的2倍[1],已获批用于晚期初治和铂敏感复发性卵巢癌的维持治疗,无论患者是否有DDR缺陷。此前研究证实尼拉帕利与免疫检查点抑制剂联用具有协同抗肿瘤活性。
临床前研究中,PARP抑制剂联合CTLA-4单抗比PD-1单抗更有效。因此,本研究[2]将探索尼拉帕利联合纳武利尤单抗(抗PD-1)或联合伊匹木单抗(抗CTLA-4)用于铂敏感晚期胰腺癌维持治疗的疗效,无论是否合并DDR通路基因突变。
二、方法
1、研究设计
开放标签、随机、Ib/II期试验,在美国宾夕法尼亚大学Abramson癌症中心完成。

2、统计假设
在研究设计时,已发表研究中胰腺癌维持治疗6个月PFS率为22%。本研究假设:此结果的2倍有临床意义。因此,研究的零假设为6个月PFS率等于44%。双侧备择假设为每个研究组的6个月PFS率不等于44%,优效性为60%,劣效性为27%。通过Kaplan-Meier曲线估计中位PFS和OS。数据截止时间为2022年1月25日。
3、DDR通路基因突变
DDR通路基因突变包括:BRCA1, BRCA2, PALB2, ATM, FANCA, FANCC, RAD50, RAD51, RAD51C, RAD51D, ATR, CHEK1, CHEK2, BARD1, BRIP1, NBN,BAP1, BLM, FAM175A, RTEL1, MRE-11, ARID1A。
三、结果
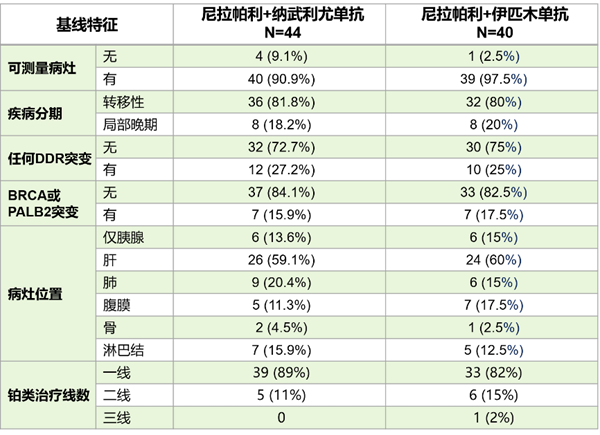
1、基线特征
2018年2月7日至2021年10月5日,91例患者被随机分配并接受至少一次药物干预(安全性分析人群),其中84例患者完成至少一次肿瘤学评估(尼拉帕利+纳武利尤单抗44例,尼拉帕利+伊匹木单抗40例)。
83%患者无致病性BRCA或PALB 2突变,74%患者无任何DDR基因突变。
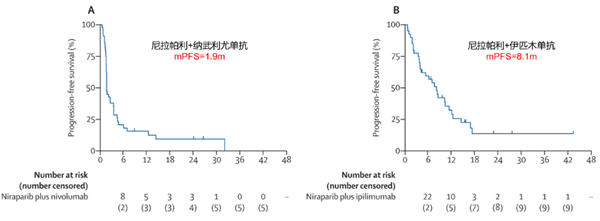
2、研究终点:6个月PFS率和mPFS
数据截止时(2022.01.25),3例患者仍在接受尼拉帕利+纳武利尤单抗治疗,8例患者仍在接受尼拉帕利+伊匹木单抗治疗。中位随访时间为23个月。尼拉帕利+纳武利尤单抗组6个月PFS率为20.6% (95%CI 8.3–32.9;与零假设相比p=0.0002),事后mPFS为1.9个月 (95%CI 1.4–2.3)。由于95%CI上限不包括零假设44%,因此该联合治疗为劣效的。
尼拉帕利+伊匹木单抗组6个月PFS率为59.6% (95%CI 44.3–74.9;p=0.045),事后mPFS为8.1个月 (95%CI 5.5–10.6)。由于95%CI下限超过了零假设44%,因此该联合治疗为优效的,达到了主要研究终点。
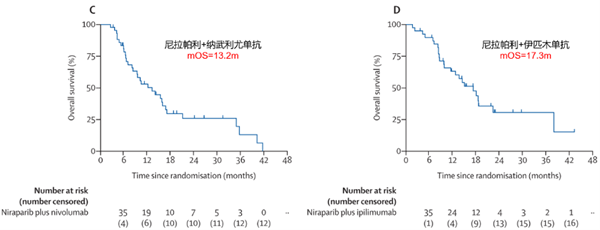
3、次要研究终点:总人群mOS和无DDR突变人群mPFS和mOS
数据截止时55例患者死亡,尼拉帕利+纳武利尤单抗31例,尼拉帕利+伊匹木单抗24例。尼拉帕利+纳武利尤单抗组mOS为13.2个月(95%CI 8.1-16.7),尼拉帕利+伊匹木单抗组mOS为17.3个月(95%CI 12.8-21.9)。
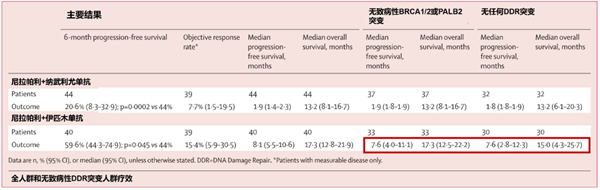
尼拉帕利+伊匹木单抗在无致病性BRCA 1/2或PALB 2突变的患者中,mPFS为7.6个月(95%CI 4.0-11.1),mOS为17.3个月(95%CI 12.5-22.2);无任何DDR突变患者中,mPFS为7.6个月(95%CI 2.8-12.3),mOS为15个月(95%CI 4.3-25.7)。
4、安全性
尼拉帕利+纳武利尤单抗组中22%患者出现3级及以上治疗相关不良反应,其中最常见的是高血压(8%)、贫血(4%)和血小板减少(4%)。1例患者出现3级免疫介导不良反应(结肠炎)。
尼拉帕利+伊匹木单抗组中50%患者出现3级及以上治疗相关不良反应,最常见的是疲劳(14%)、贫血(11%)和高血压(9%)。6例患者出现3级免疫介导不良反应,包括皮疹(3例)、肺炎(2例)和结肠炎(1例)。
四、讨论
■ 尼拉帕利联合伊匹木单抗维持治疗能够突破DDR基因突变限制,实现全人群获益:此前奥拉帕利POLO研究[3]中入组gBRCA突变晚期胰腺癌患者,mPFS为7.4个月,但gBRCA突变在胰腺癌中仅为4~7%。本研究探索了尼拉帕利联合免疫检查点抑制剂在全人群的疗效。尼拉帕利+伊匹木单抗用于晚期胰腺癌患者维持治疗的6个月PFS率达59.6%。对缺乏任何DDR突变的患者中,二者联合也展示出了抗肿瘤活性,mPFS为7.6个月,mOS为15个月。
■ 非细胞毒性药物维持治疗可能优于细胞毒性药物:既往研究FOLFIRINOX 治疗4个月后,以氟尿嘧啶/亚叶酸钙维持治疗的mPFS为5.1个月[4];继续接受FOLFIRINOX治疗的mPFS为5.5个月,mOS为14.7个月[5]。尼拉帕利+伊匹木单抗组mPFS为8.1个月,mOS为17.3个月,均显示更长。
■ 相比联合PD-1单抗,尼拉帕利联合伊匹木单抗疗效更优:在全人群和亚组分析中,尼拉帕利+伊匹木单抗组的mPFS、mOS和ORR数值均高于尼拉帕利+纳武利尤单抗组,且可信区间不重叠。95%CI不重叠提示治疗组之间可能存在差异,但本试验未进行两组间的直接比较。动物试验观察到,PARP抑制剂联合抗CTLA-4比联合抗PD-1更有效,表现为PARP抑制剂+抗CTLA-4治疗后肿瘤内效应T细胞增加。
■ 联合治疗患者耐受性良好:本研究中与尼拉帕利、伊匹木单抗和纳武利尤单抗相关的不良事件与既往研究相似。尼拉帕利无论联合PD-1单抗还是联合CTLA-4单抗,患者耐受性均良好。
■ 此前PARP抑制剂胰腺癌维持治疗中,奥拉帕利和芦卡帕利仅对BRCA 1/2或PALB 2突变的患者有效,此类患者PARP抑制剂联合免疫检查点抑制剂的疗效尚不明确,正在开展的其他研究将回答这一问题。
专家点评
■ 局部晚期或转移性胰腺癌预后差,5年生存率低,被称为“癌中之王”。延长姑息性化疗时间可能会导致化疗耐药和累积毒性。维持治疗的策略是使用低毒性药物来延缓临床症状恶化和延缓疾病进展,保证患者生活质量。该研究显示尼拉帕利联合伊匹木单抗疗效优于尼拉帕利联合纳武利尤单抗,不良反应可以接受,为临床应用提供了参考。
■ 相比既往研究,本研究的优势在于扩大了应用人群,没有DDR突变的患者也能获益,推测可能原因一是尼拉帕利PARP酶捕获能力更强,在卵巢癌维持治疗中已经突破了DDR限制,二是尼拉帕利联合伊匹木单抗有一定的协同抗肿瘤效应。
■ 既往奥拉帕利仅对BRCA突变的胰腺癌患者进行了疗效探索。与之不同的是,尼拉帕利在卵巢癌治疗中BRCA野生型也能获益,在本研究中联合CTLA-4单抗也覆盖了全人群,未来需要探索这种联合治疗与PARP抑制剂单药以及细胞毒性药物维持治疗疗效的比较。

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
