随着分子靶向药物PARP抑制剂的问世,初诊晚期卵巢癌的治疗模式逐渐已由既往的“手术+化疗+观察随访”模式转变为“手术+化疗+维持治疗”新模式,以期为患者争取更长的生存获益。
近年来,随着越来越多PARP抑制剂一线维持治疗3期注册临床研究结果公布,究竟研究之间如何对比也成为了临床专家关注的热点问题。
本期特别邀请来自安徽医科大学第二附属医院卫兵教授解读一篇题为《Feasibility Study of a Network Meta-Analysis and Unanchored Population-Adjusted Indirect Treatment Comparison of Niraparib, Olaparib, and Bevacizumab as Maintenance Therapies in Patients with Newly Diagnosed Advanced Ovarian Cancer》,并于2022年3月刊登在Cancers (Basel) 的文章(IF:6.639),着重阐述了一线维持治疗相关研究之间进行间接治疗比较的可行性。


 00:000:00 音频
00:000:00 音频 一、研究背景
基于严格设计的随机对照试验(RCTs)的药效直接比较,被认为是评价干预措施疗效的更可靠证据。但是,很多时候我们无法通过RCT来直接比较药效。这时,我们需要根据可获得的实验数据采用间接比较(indirect treatment comparison,ITC)来分析干预措施的相对疗效。
治疗的间接比较方法必须遵循统计学原则,以确保相似试验之间比较的公平性。通常基于可获得数据类型,选择不同治疗的间接比较方法。这篇文章探讨了采用网络荟萃分析(Network meta-analysis,NMA)和人群校正的治疗间接比较(population-adjusted ITC,PAIC),来评价尼拉帕利和其他药物在一线维持治疗疗效比较的可行性。
二、研究方法
影响方法选择的关键因素可分为如下3点:
● 个体数据(individual patient data,IPD)的可获得性!
● 所有研究的治疗组/对照组是否能构成网络?
● 是否存在不同试验之间人群特征变量之间的差异?
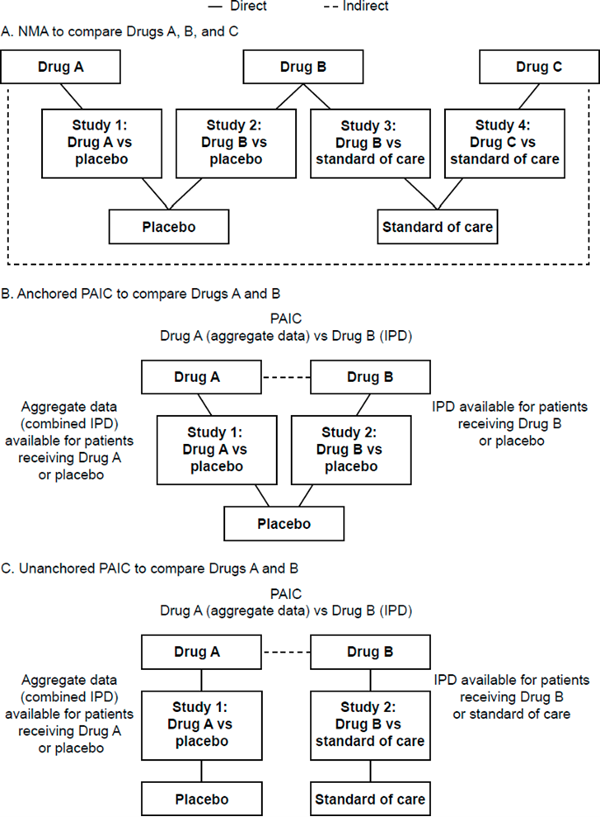
当研究者关于需要对比的药物都只有研究汇总性数据时,可以选择NMA方法,该方法是基于间接比较或间接比较与直接比较合并结果、同时分析多个干预措施的Meta分析(图A)。此外,当研究者仅有干预药物的IPD和对照药物汇总性数据时,则可以选用人群校正的治疗间接比较。这种情况往往在实际应用中最为常见,比如,企业往往有自己研发药物的IPD,所以只能通过该方法(图B、C)。
三、研究结果
1、NMA可行性评估
筛选12项一线维持治疗的RCT(PRIMA、SOLO1、PAOLA-1、GOG218、ICON7、VELIA、CHIVA、AGO-OVAR12、TRINOVA-3、MIMOSA、AGO-OVAR16、NCT01227928)如图1所示。
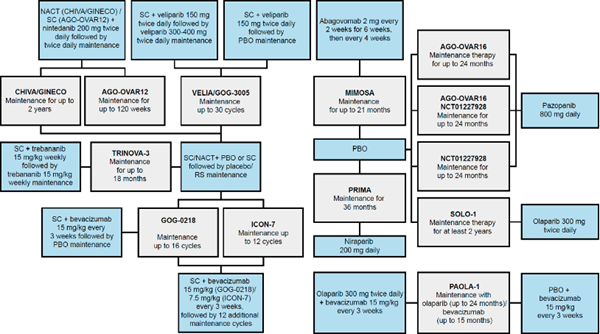
图1:针对NMA可行性确定的12项RCT
这12项研究包括了尼拉帕利在内的3个PARP抑制剂,酪氨酸激酶通路抑制剂、抗血管生成药物等。对比后发现,其实验设计、入组人群、结局指标均存在差异,不符合NMA评估标准(图2)。
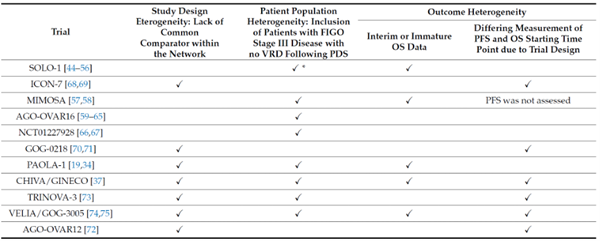
图2:不符合PRIMA研究的NMA评估标准(不符合的标注“√”)
2、PAIC可行性评估
PAIC比较的是PAOLA-1和PRIMA研究,考虑到2个实验的对照组不同,因此采用非锚定的PAIC方法(图3)。

图3:针对PAIC可行性确定的2项研究
这2项研究在实验设计方面存在一些相似,但是在实验结局、入选/排除标准、研究前使用贝伐以及行NACT的情况方面存在显著差异,因此采用非锚定的PAIC也不可行:
● 入选/排除标准:
在PAOLA-1中,有一半以上的患者(接受奥拉帕利联合贝伐珠单抗(54%)或贝伐珠单抗单药(52%))在PDS后无疾病证据。然而,在PRIMA中,FIGO III期的患者在行PDS后必须有肉眼残留病灶才可以入组研究。因此,与PAOLA-1相比,PRIMA中的患者预后“更差”,这也使得无锚定的PAIC不可行。尽管最近发表的PAOLA-1高危人群似乎与PRIMA人群更相似,但许多因素影响该方法,例如PFS时间评估频率的差异以及既往贝伐珠单抗联合化疗的使用,如下所述。
● 入组前接受贝伐珠单抗治疗:
PAOLA-1中的患者必须在进入研究前对贝伐珠单抗联合铂类药物化疗有应答,之后进行贝伐珠单抗联合奥拉帕利或安慰剂的维持治疗。而PRIMA中的少数患者(n = 7)在开始尼拉帕利维持治疗前接受了贝伐珠单抗治疗。两项研究之间的这种差异是潜在的混杂因素。
3、接受新辅助化疗(NACT)情况
在PRIMA中,66%的意向治疗组和67%的BRCA突变患者接受了NACT。但是,但是PAOLA-1中未报道接受NACT的患者比例。NACT的使用被确定为该分析的潜在混杂因素,因此,进行两者的间接比较时,接受NACT患者的比例应当相似。
4、PFS评估方法和评估周期
PRIMA的主要终点为BICR评估的PFS,而PAOLA-1的主要终点为研究者评估的PFS,这两类评估可能存在差异。此外,PRIMA中更频繁的扫描间隔(每12周进行一次)可能导致中位PFS估计值短于PAOLA-1(每24周进行一次扫描,或如果有疾病进展证据,每12周进行一次扫描),同样会产生偏倚。
四、专家点评
■ 由于各大临床研究的实验设计、入组人群、结局指标均存在差异,无法与PRIMA进行网络荟萃分析。
■ PAOLA-1和PRIMA的非锚定PAIC也不合适,其原因是实验结局、入选/排除标准、研究前是否使用贝伐以及行NACT的情况方面存在显著差异。
■ 治疗的间接比较方法必须遵循统计学原则,以确保相似试验之间比较的公平性。
■ 基于国内现状,尼拉帕利单药无论BRCA/HRD状态均获得NMPA批准用于初治晚期卵巢癌的一线维持治疗,奥拉帕利单药仅限于BRCA阳性人群。

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
