本期OC文献精读特邀中国医学科学院肿瘤医院深圳医院的孙力教授,与大家分享一篇2022年4月刊登在Lancet(IF=79.32)杂志的文章:Endometrial cancer.


 00:000:00 音频
00:000:00 音频
一、流行病学
子宫内膜癌是女性中第六大常见癌症,2020年全球有417,000例新发病例。女性终生患内膜癌的风险约为3%,中位确诊年龄为61岁。过去30年中,总发病率上升了132%,主要是危险因素是肥胖和人口老龄化。内膜癌发病率最高是北美(图1)。尽管所有年龄组的发病均有所增加,但40岁以下女性的病例新增了一倍。
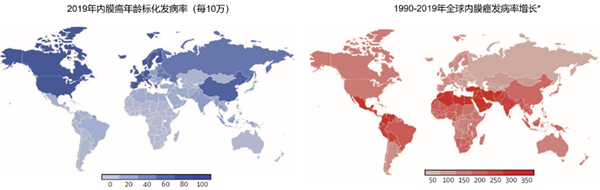
图1:内膜癌全球疾病负担
*表示ASIR变化百分比,即2019年ASIR除以1990年ASIR乘以100。ASIR:age-standardised incidence rate 年龄标化发病率
二、临床表现
早期表现为绝经后出血,但特异性仅5-10%。内膜癌导致绝经后出血在50岁以下女性低于1%,55岁以上女性中上升到3%,80岁以上女性中上升到24%。英国国家卫生与保健优化研究所(NICE)建议55岁以上女性出现绝经后出血应立即检查。绝经前女性主要症状是月经增多、经期延长或月经间期出血,但特异性仅0.3%。应警惕年轻女性的高危因素,如家族史、肥胖和多囊卵巢综合征(PCOS)。局部晚期内膜癌可能出现腹胀、疼痛和泌尿或肠道功能障碍。在高达50%的内膜癌病例中,宫颈细胞学存在非典型腺细胞,在宫颈癌筛查中可能是一个提示。
三、危险因素
1、肥胖、代谢和生殖因素
内膜癌患病风险随年龄和BMI的增加而增加。肥胖会增加内膜癌风险(图2)。雌激素暴露过多的生殖因素,如月经初潮过早(< 12岁)、绝经延迟(≥55岁)、无排卵(如PCOS)和未生育也会增加内膜癌风险。长期服用他莫昔芬会导致内膜癌风险增加4倍。胰岛素抵抗和高胰岛素血症会增加雌激素和胰岛素样生长因子(IGF)-1的生物利用度,促进内膜增殖,通过直接和间接途径激活PI3K–AKT–mTOR致癌信号通路。
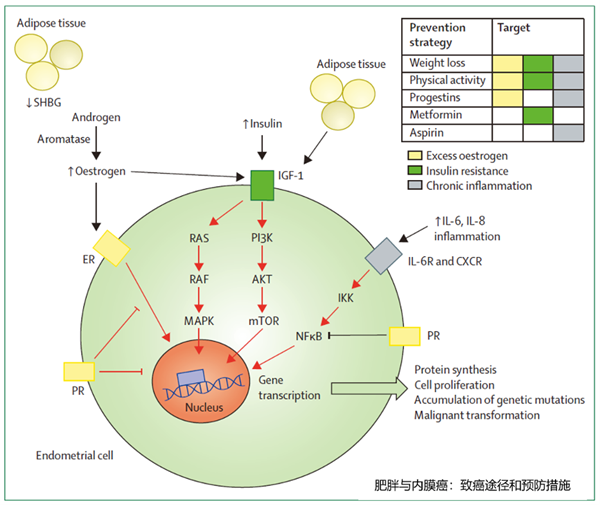
图2 肥胖相关内膜癌:致癌途径和预防措施
2、遗传因素
林奇综合征( Lynch syndrome):错配修复(MMR)基因MLH1、MSH2、MSH6和PMS2的遗传致病性突变将导致13-49%的终生内膜癌风险,也会增加结肠直肠癌,卵巢癌和其他多种癌症的风险,推荐所有内膜肿瘤进行MMR检测(图3)。考登综合征(Cowden syndrome):PTEN抑癌基因的罕见致病性突变将导致20-30%的终生内膜癌风险。BRCA1/2致病性突变略微增加浆液性子宫内膜癌的风险,报道尚无定论。与内膜癌有一级亲属关系的女性,患病风险也会增加一倍,可能与单核苷酸多态性有关。
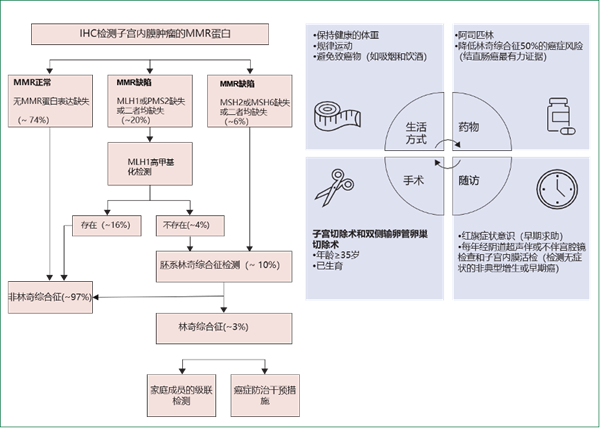
图3:林奇综合征相关内膜癌的筛查、诊断和降低风险策略
四、诊断
诊断依赖于内膜组织活检,但侵入性检查仅适用于经阴道超声检查提示内膜病变或内膜增厚的患者,绝经后女性使用5 mm的阈值检测灵敏性为96.2%,阴性预测值为99.3%,但特异性仅为51.5%,需要额外检查才能排除内膜病变(图4)。经阴道超声、宫腔镜检查和内膜取样的一站式检查可以最大程度地减少诊断延误。创新诊断方法可以评估哪些高危女性需要侵入性检查,同时保证低危女性筛查的安全性和便利性(图5)。术前MRI扫描可以评估肌层侵犯程度、盆腔淋巴结和宫外疾病。胸部、腹部和盆腔CT检查可用于评估高级别内膜癌的宫外侵犯或转移。
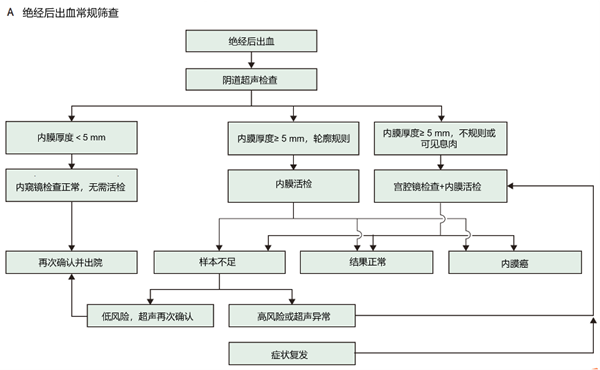
图4:常规内膜癌诊断方法
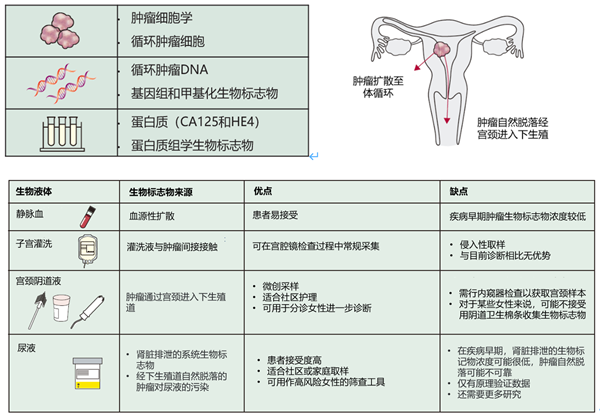
图5:内膜癌创新诊断方法
五、病理与分子分型
病理学类型包括:子宫内膜样癌;浆液性癌;透明细胞癌;未分化癌;混合细胞癌;癌肉瘤;中肾腺癌;鳞状和黏液性癌。
分子分型包括:
● POLE超突变型:患者主要为年轻女性,预后较好,复发率低,死亡率低于1%;
●MMR缺陷型(MMRd):微卫星不稳定型,约10%发生在Lynch综合征的背景下。预后中等,具有分期依赖性;
●高拷贝型(p53突变):TP53突变、广泛的体细胞拷贝数改变和低突变率。以浆液性癌、癌肉瘤和低级别内膜癌常见,约占所有内膜癌的20%,但死亡率占比50-70%;
●低拷贝型(无特异性分子谱,NSMP):排除性诊断。预后依赖于分期和组织形态学。
六、手术
■ 主要术式:全子宫切除和双侧输卵管-卵巢切除术。绝经前的早期患者可以考虑保留卵巢,对生存结局没有影响。
■ 微创子宫切除术住院时间更短,失血量、疼痛和围手术期并发症发病率更低,是早期病变的首选术式。
■ 机器人手术相比腹腔镜肿瘤学结局相似,住院时间更短、转开腹率更低,但价格昂贵。
■ 举宫器使用是否会增加复发风险尚有争议。
■ 早期病变存在麻醉或开腹手术禁忌时,可以考虑行经阴道子宫切除,伴或不伴双侧输卵管-卵巢切除。
■ 侵犯宫外的肿瘤手术选择需考虑转移灶位置、完全细胞减灭术可能性和患者适应性。III-IV期经初始细胞减灭术(PDS)能达到R0的患者,生存结局显著改善。新辅助治疗联合间歇细胞减灭术(IDS)与PDS的次优切除相比,围手术期发病率降低,生存率相当,与单纯化疗相比,生存结局得以改善。
■ 侵犯宫颈的II期患者根治性子宫切除相比单纯切除没有生存获益,对II期患者来说,辅助治疗与肿瘤结局更相关。
■ ESGO–ESP–ESTRO和NCCN 2021指南推荐II期和III-IV期能达到R0切除的患者进行PDS。
■ 复发性内膜癌手术需要考虑从最初诊断到复发的时间、复发的位置(可切除性)、病灶数量和患者状态,只有达到完全减瘤才有生存获益。
七、保留生育手术
未完成生育的不典型内膜增生和内膜癌患者保留子宫的需求逐渐增多。接受大剂量口服孕激素和/或宫内孕激素治疗内膜不典型增生缓解率约为65%,低级别早期内膜癌缓解率为50%。高级别内膜癌、肌层浸润和附件肿块的患者不适合保留生育功能,建议评估分子分型指导治疗。激素治疗的反应需要6-12个月或更长时间,应密切监测。保宫者肿瘤复发率高达35%,妊娠结局可能不理想。建议在生育完成后行子宫切除术。
八、淋巴结清扫和前哨淋巴结活检
■ 常规淋巴结清扫术没有明显生存获益。但淋巴结评估可用于手术分期、指导辅助治疗和提示预后。需要权衡盆腔和腹主动脉旁淋巴结清扫术的围手术期并发症发病率,包括潜在的长期下肢淋巴水肿。
■ 使用示踪剂Tc99m或FDA批准的染料进行前哨淋巴结活检(SLNB),其安全性、阳性检出率和阴性预测值均较高(97-99%),减少了不必要的淋巴结清扫。
■ Meta-analysis证实高级别肿瘤患者使用SLNB检测淋巴结转移的准确度高、假阴性率低(8%),与低级别肿瘤相当。
■ 前哨淋巴结的病理超分期比常规切片检测到更多的转移,包括微转移和孤立的肿瘤细胞。
■ 转移高风险患者建议行网膜取样和/或腹膜活检。
九、辅助治疗
■ 2/3的内膜癌患者为Ⅰ期,多数预后极佳。但也存在结局相对较差的患者,高危患者需要强化治疗,低危患者可能从降级治疗中获益。
■ IA期低级别患者的复发风险较低(< 5%),不需要额外治疗。
■ 中等复发风险患者可以使用阴道近距离放疗,耐受性良好,能将阴道复发率从14%降至2%以下。
■ 中、高复发风险患者伴淋巴脉管间隙浸润(LVSI)或高级别肿瘤时,可选择外照射放疗。全面手术分期且无LVSI,可选择阴道近距离放疗。
■ p53突变肿瘤联合化疗有明显获益(59% vs 36% RFS)。NSMP肿瘤也显示获益,但程度较小(80% vs 68% RFS)。MMRd肿瘤患者未从化疗中获益(68% vs 76% RFS),而POLE突变肿瘤患者伴或不伴化疗的结局都极佳(100% vs 97% RFS)。因此,POLE突变肿瘤患者可以考虑降级治疗。
■ 免疫检查点抑制剂可能使MMRd肿瘤患者获益。
十、晚期和复发性疾病
■ 晚期不可切除性或多灶复发性内膜癌采用姑息性治疗。
■ 标准一线化疗方案为卡铂联合紫杉醇,无进展生存期为13个月。
■ ER/PR阳性肿瘤采用激素治疗耐受性良好,口服孕激素的缓解率超过35%。芳香化酶抑制剂单药改善生活质量,临床获益率40-45%,但缓解率仅10%。
■ 局部复发和寡转移采用根治性放疗局部控制率高达90%,立体定向放疗法直接照射肿瘤,可持久控制疾病。
■ mTOR抑制剂单药缓解率仅10%,依维莫司联合来曲唑缓解率为28-32%,对PR阳性患者缓解率为45%。
■ 免疫检查点抑制剂用于MMRd肿瘤:pembrolizumab(缓解率57%),dostarlimab(缓解率42%)。非MMRd肿瘤:pembrolizumab + lenvatinib(MMR proficient缓解率36%, MMRd缓解率63.6%),但耐受性值得关注,2/3患者出现3级以上治疗相关不良反应。
■ 抗HER2单抗:HER2在1/4的TP53突变内膜癌中过表达,Ⅲ/Ⅳ期或复发的HER2阳性肿瘤采用卡铂紫杉醇+曲妥珠单抗+曲妥珠维持治疗,可以提高PFS和OS。
■ PARP抑制剂:TP53突变肿瘤中15-53%存在同源修复缺陷(HRD),PARP抑制剂治疗可能获益。

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
