对于晚期上皮性卵巢癌的初始治疗,是直接进行初始肿瘤细胞减灭术,还是选择新辅助化疗+间歇性肿瘤细胞减灭术?对于临床中日益增多的新辅助化疗的使用,是否可对患者生存造成影响?目前仍有许多问题存在争议。本期文献精读栏目就新辅助治疗的问题,特别邀请来自天津市中心妇产科医院的孙培松教授解读2021年9月发表在JAMA Oncol上的一篇文章,《Association Between Overall Survival and the Tendency for Cancer Programs to Administer Neoadjuvant Chemotherapy for Patients With Advanced Ovarian Cancer》。


 00:000:00 音频
00:000:00 音频 一、研究背景
自2010年EORTC 55971研究结果证实,对于晚期上皮性卵巢癌,新辅助化疗(NACT)联合间歇性肿瘤细胞减灭术(IDS)与初始肿瘤细胞减灭术(PDS)相比,有相似的生存结局,并且可提高R0切除率,降低围手术期的并发症。尽管如此,目前关于NACT的合理使用仍存在较大争议,一些观察性研究发现,接受NACT的患者总生存要低于PDS的患者,怀疑其可能影响患者总生存。虽然有这些担忧,随着后续临床试验的相继公布,仍有越来越广泛的患者接受NACT。
二、研究目的
本研究使用国家癌症数据库的患者数据,旨在评估晚期卵巢癌患者使用高水平的NACT与OS之间的相关性。
三、研究方法
纳入2004年1月至2015年12月诊断为IIIC或IV期的上皮性卵巢癌,包括浆液性、粘液性、子宫内膜样、透明细胞或其他腺癌组织学。以2010年发表的第一篇证实NACT非劣效于PDS的随机临床试验(2010年NEJM EORTC 55971)作为分界线,将2004-2009年归类为NACT广泛使用前,2010-2015归类为NACT广泛使用期。按照一定的统计学方式分为新辅助化疗高水平组及新辅助化疗低水平组。数据在2020年9月至2021年1月进行分析。
四、统计学方法
01、癌症项目分类
首先根据患者年龄、种族、Charlson合并症指数(0、1、2分)、肿瘤组织学类型(浆液性、粘液性、透明细胞、子宫内膜样或其他腺癌)、肿瘤分期(IIIC、IV期)、分级(1、2、3或未知)、保险情况(未投保、私人、医疗保险、医疗补助、政府计划或未知)、诊断年龄、收入等一系列指标,使用多元logistic回归模型,预测每个患者接受NACT的概率。
对于每个癌症项目中的卵巢癌患者,将其预测的接受NACT的概率求和,估计此癌症项目中接受NACT的预期患者数。
当观察到实际接受NACT的患者数超过预期数量时,将此癌症项目归类为NACT的高水平组;低于预期数量时归类为NACT的低水平组。
02、癌症项目匹配
使用广义精确匹配法将2010年前后有相似NACT治疗模式的病例进行匹配。在322个癌症项目中,识别出19562名患者接受了高水平新辅助治疗方案,19737名患者接受了低水平的治疗方案(图1)。
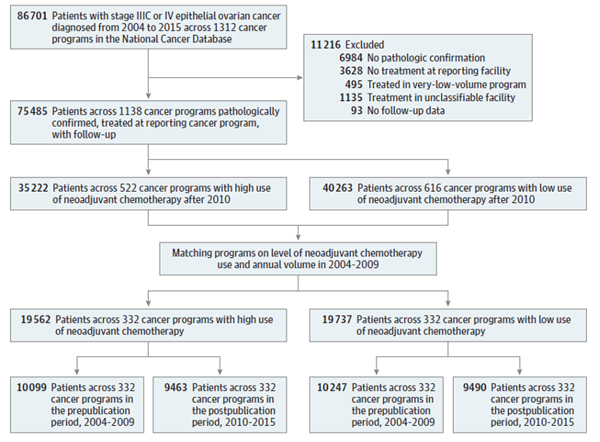
图1 研究流程图
五、研究终点
病例组合标准化的中位OS;使用灵活参数生存分析模型评估的1年全死因死亡率。
六、研究结果
01、在2010年以前,高低水平的NACT使用情况相似,在2010年后两者出现较大差异(图2)。
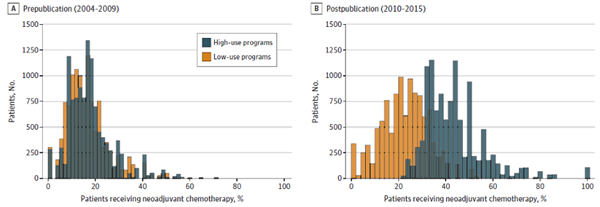
图2 美国癌症患者接受高低水平NACT的频率
研究确认了接受治疗的19562名患者接受高水平的NACT(中位年龄[SD],63.9岁[12.6];3.2%亚裔,8.0%黑人,4.8%西班牙裔,82.5%白人),2004-2009年使用率为21.7%,在2010-2015年间提高到42.2%。19737名患者接受低水平的NACT(中位年龄[SD],63.5岁[12.6];3.1%亚裔,7.7%黑人,6.5%西班牙裔,81.8%白人),使用率同样略有增加,从20.1%增至22.5%。
02、高水平与低水平NACT组,标准化的中位OS改善相似。
高水平组从31.6m(IQR,12.3-70.1m)提升至37.9m(IQR,17.0-84.9m);(差值6.3m;95%CI,4.2-8.3m)。
低水平组从31.4m(IQR,12.1-67.2m)提升至36.8m(IQR,15.0-80.3m);(差值5.4m;95%CI,3.5-7.3)。
高水平组和低水平组的标准化mOS无明显差异(difference-in-differences,0.9months;95%CI, ?1.9 to 3.7)。
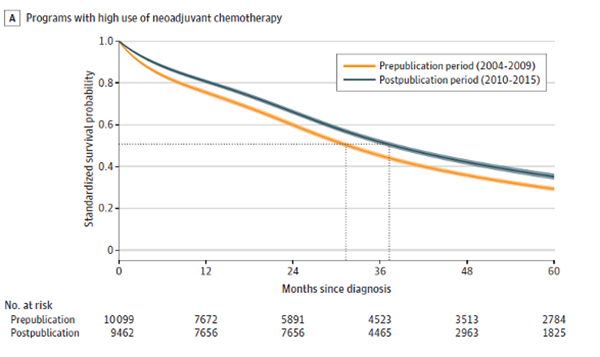
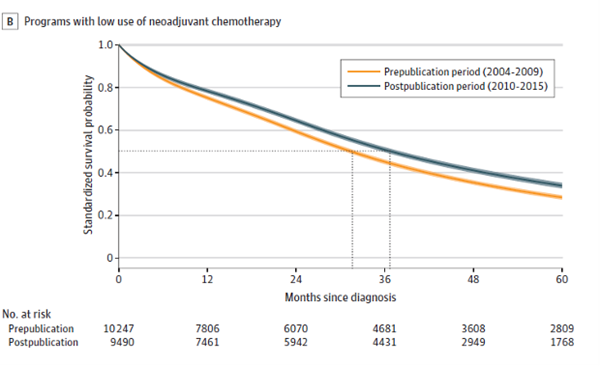
图3 标准化的OS分析
03、接受高水平NACT的患者早期死亡率降低更多(图4),这种改善使得高水平组术后30天和90天的死亡率同样下降更多(表1)。
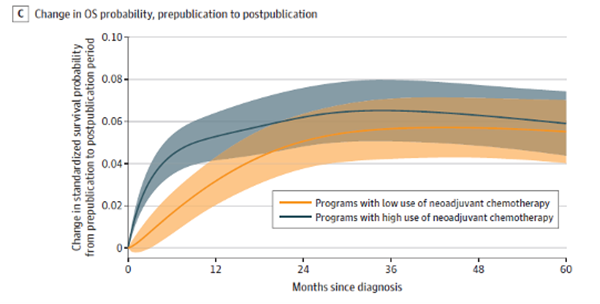
图4 高低水平NACT的标准化OS分析
04、对于一年死亡率,低水平组(从24.9%至21.8%;风险差,-3.2%,95%CI,-4.3至-2.0),高水平组(从25.6%至19.3%;风险差,-5.2%;95%CI,-6.4至-4.1),两组间差异(difference-in-differences,-2.1%;95%CI,-3.7至-0.5),高水平组同样下降更多(表1)。
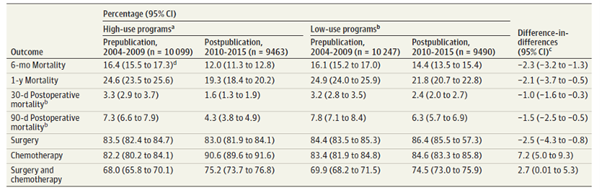
表1 高低水平NACT的次要终点分析
七、结论与讨论
在这项观察性研究中,验证了在EORTC 55971研究结果发布后,真实世界中NACT的使用情况发生了显著改变。利用统计学方式对比高低水平NACT的差异,结果显示高水平组可降低早期死亡风险,且不会影响患者总生存期。
迄今有4项III期RCT研究对比NACT与PDS,均证实NACT可提高理想手术比例,降低手术相关发病率和死亡率,且不影响总生存。但因研究设计的局限性,两者的使用仍存在争议,第五项TRUST研究(NCT02828618)将进一步验证PDS与NACT的OS获益差异,目前已结束入组,结果将于2023年公布。
关于术前新辅助化疗的使用有哪些重要的限制因素,对卵巢癌的分型、分期、个人因素有哪些要求目前仍不清楚,因此精准的评估和选择NACT的获益人群在疾病的诊疗中至关重要。
八、专家点评
对于晚期卵巢上皮性癌患者初始治疗该如何选择,是NACT还是PDS目前仍存在争议,但无论NACT还是PDS,都应以手术达到R0切除作为治疗目标。估计能够达到满意减瘤的,可考虑行PDS;估计无法手术或满意减瘤可能性较低的,可考虑先予NACT。
目前随着NACT在临床中应用愈发广泛,针对NACT是否可延误手术时机,影响预后的质疑也愈加增多。本研究使用独特的统计学方法,回顾性收集了2004-2015年的患者数据,验证了新辅助化疗的广泛使用并未对总生存造成负面影响。
综上来看,确定晚期卵巢癌的最佳治疗方式,仍需医生充分评估手术R0切除可能性、手术复杂程度和围术期严重并发症风险等因素,制定精准的个体化治疗方案。

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
