各位妇瘤同仁大家好,欢迎收听本期OC文献精读,我是今天的领读人,来自四川省肿瘤医院、电子科技大学医学院附属肿瘤医院的王登凤医生,今天与大家分享的文章是2021年1月刊登在《Gynecol Oncol Rep》杂志的文章:卵巢癌中的PARPAi after PARPi


 00:000:00 音频
00:000:00 音频 01、文章概述
上皮性卵巢癌的治疗形势正在迅速变化。PARPi现已批准用于一线维持治疗以及复发性卵巢癌的治疗和维持。许多临床试验将之前使用过PARPi的患者排除在参与范围之外,因此,没有关于患者在前线治疗中使用过PARPi,且再次使用PARPi的疗效或安全性的数据。既然PARPi已被批准用于更多的患者,那么使用PARPi后再次使用的机会是存在的。
今天精读的文献是一项多中心回顾性研究,入组患者为接受过≥2线包含PARPi治疗的上皮性卵巢癌患者。22例患者符合纳入标准。收集的变量包括年龄、细胞减灭术的详情、一线化疗、首次复发和治疗、首次和第二次开始使用PARPi的日期、使用PARPi后复发日期、最佳应答、剂量中断、剂量调整、毒性、生命体征状态和最后一次随访日期。主要使用Fisher精确检验进行分析,以评估PARPi1和PARPi2之间的毒性相关性、对PARPi1和PARPi2的最佳应答相关性以及BRCA状态与对PARPi1和PARPi2的应答相关性进行了描述。
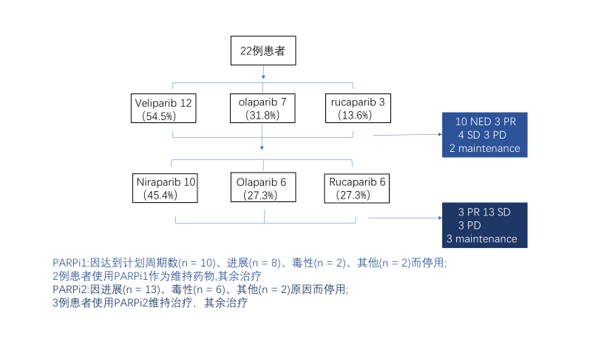
入组的22例患者中,由于初次使用PARPi时治疗方式不一,故无法对其最佳应答进行评估。而第二次使用PARPi治疗方式更一致,19名患者均使用PARPi作为治疗手段,这其中没有过任何患者达到CR,3名部分缓解,这3名患者均有BRCA突变且均使用PARPi1作为一线治疗。这是否可以提示我们BRCA突变人群一线使用PARPi之后对再使用PARPi有更好的应答。因此作者又对BRCA突变人群进行了细分,在第二次使用PARPi时,有3例患者达到PR、8例SD和2例PD。作者认为这是应该在BRCA突变人群中对PARPi进行rechallenge的信号。另外值得注意的是,有8名患者因疾病进展而停用PARPi1。这8名患者对PARPi1的最佳应答中有:2名PR、2名SD、3名PD,1名患者由于使用PARP维持治疗不能作为评估。而这些患者对PARPi2的最佳应答为5名SD,3名PD。尽管这8名患者都因疾病进展而中止了第1次使用PARPi,但仍有5名患者在第二次使用PARPi时以SD形式获得了临床获益。并且这些应答是持久的,其中3名在PARPi2开始后保持无进展状态超过12个月,最长达到18.3个月。所以,也许第一次使用PARPi进展了,并不代表再次使用PARPi就不能获益。在这个研究中,最常见G3/4毒性为血液学毒性。初始使用PARPi后的毒性与第二次使用PARPi后的毒性无显著相关性(p > 0.05)。未发生AML/MDS。
02、结论
综上,作者得出结论:前线使用PARPi不一定会对后续使用PARPi产生耐药,在复发情况下似乎是一种安全的选择。一些患者能够从使用PARPi再治疗中获益,特别是把PARPi1作为一线治疗时疾病未进展的BRCA突变的肿瘤患者。此外,接受PARPi1治疗直至进展的患者依然对PARPi2治疗应答并产生了一定的临床获益,这表明耐药性的产生不一定与先前的PARPi使用和疾病进展相关。此外,初次使用与第二次使用PARPi后的毒性无显著相关性。作者同时提出,如何辨别哪些患者能从PARPi再治疗中获益,是否可以预测重复使用PARPi可能受益的患者,是否可以使用联合疗法来克服获得性铂耐药,在PARPi耐药的时候单一疗法和联合疗法如何选择等等问题都有待我们继续去探索和思考。
附原文
1.介绍
上皮性卵巢癌(EOC)的治疗形势正在迅速变化。随着PAOLA-1、PRIMA和VELIA对PARPi作为一线维持治疗的研究数据发布 (Moore,2018;科尔曼,2019年;Gonzalez-Martín,2019年;Ray-Coquard,2019 ),PARPi现已批准用于一线维持治疗以及复发性EOC的治疗和维持。
许多临床试验将之前使用过PARPi的患者排除在参与范围之外,因此,参与过PARPi早期临床试验的患者无法参与针对复发性疾病的近期试验。既然PARPi已被批准用于更多的患者,那么使用PARPi后再次使用PARPi的机会是存在的。截止目前,我们没有关于患者在前线治疗中使用过PARPi,且再次使用PARPi的疗效或安全性的数据。
与细胞毒性化疗药物的再使用非常相似,对于特定患者,无疑会有决定PARPi再使用时间点的影响因素。其中可能包括既往使用PARPi的时间、对既往PARPi的应答或在既往使用PARPi时是否进展、肿瘤的分子特征(包括乳腺癌基因(BRCA)状态或同源重组缺陷(HRD)状态);但也可能包括损伤DNA能力丧失的其他决定因素,甚至可能包括丢失测试患者是否产生PARPi耐药性的能力。为了评估这些决定因素,OReO (NCT03106987)等临床试验对于明确重复使用单一疗法PARPi的疗效至关重要。我们的研究试图以回顾性、多中心的方式评估疗效。
2.方法
这是一项经IRB(伦理委员会)批准的多中心回顾性研究,对象为在俄克拉荷马大学健康科学中心、科罗拉多大学医学院、加利福尼亚大学洛杉矶医学中心和匹兹堡大学医学中心麦咭-妇女医院接受过≥2线包含PARPi治疗的EOC患者。
22例患者符合纳入标准。收集的变量包括年龄、关于细胞减灭术的详情、一线化疗、首次复发和治疗、首次和第二次开始使用PARPi的日期、使用PARPi后复发日期、最佳应答、剂量中断、剂量调整、毒性、生命体征状态和最后一次随访日期。不良反应是根据《不良事件通用术语标准(CTCAE)》第4.0版定义和分级的。完全缓解(CR)、部分缓解(PR)、稳定疾病(SD)和疾病进展(PD)根据RECIST v1.1标准定义。
描述性地汇总了人口统计学、临床和病理学数据,然后使用Fisher精确检验进行分析,以评估PARPi1和PARPi2之间的毒性相关性、对PARPi1和PARPi2的最佳应答相关性以及BRCA状态与对PARPi1和PARPi2的应答相关性。此外,使用Cox风险比模型确定PFS与PARPi2的比值是否与PFS与PARPi1的比值相关。
3.结果
确定了22例既往使用过PARPi的患者,并再次使用PARPi再治疗(表1)。确诊时的中位年龄为54.5岁。其中,11例患者(50.0%)有胚系BRCA突变,2例患者(9.1%)有体系BRCA突变。20例(90.9%)为高级别浆液性EOC,2例(9.1%)为混合型EOC(1例为高级别浆液性、高级别子宫内膜样混合EOC,另1例为高级别子宫内膜样混合透明细胞EOC)。17例(77.3%)为III期,20例(90.9%)接受了初始细胞减灭术。所有患者均接受含铂化疗作为其初始治疗的一部分,12名患者(54.5%)在初始化疗后接受贝伐单抗维持治疗,1名患者(4.5%)接受PARPi维持治疗。首次复发时,中位无铂间期为15.0个月(范围:2.0–48.7个月)。
对于初次使用PARPi,大多数患者接受veliparib治疗,其次是olaparib和rucaparib。9名患者接受了veliparib联合铂类、紫杉醇和贝伐单抗作为GOG9923的一线治疗。3名患者在GOG9927实验中接受了veliparib联合卡铂、脂质体阿霉素和贝伐单抗以治疗铂敏感复发卵巢癌。6例患者在二线及二线后接受了olaparib治疗,1例患者在接受一线含铂化疗后接受了olaparib维持治疗。2例患者在复发治疗后接受rucaparib作为维持治疗,1例患者在接受rucaparib作为4线治疗。对于第二次使用PARPi,大多数患者接受了niraparib治疗,其次是olaparib和rucaparib。PARPi1因达到计划周期数(n = 10)、进展(n = 8)、毒性(n = 2)而中止。

我们试图评估对PARPi1的应答是否与对PARPi2的应答相关,然而,我们的12名患者在临床试验中接受了veliparib联合化疗(但不是作为维持治疗),这使得很难将他们分为应答者和无应答者。这其中10例患者在治疗结束时并无疾病证据(NED)。此外,2名患者一开始就接受了PARPi作为维持治疗,仅剩下8名患者接受了PARPi作为治疗,可对其应答进行评估。由于患者接受初始PARPi治疗的治疗方式多种多样,因此很难对PARPi1的“最佳应答”进行分类,从而难以确定对PARPi1的反应是否能预测对PARPi2的反应。
虽然对PARPi1的“最佳应答”难以评估,但对PARPi2的应答是可评估的,因为治疗方式更一致(22名患者中有19名接受了PARPi2治疗)。PARPi2治疗没有任何患者达到任何完全缓解(CR), 有3名患者部分缓解(PR)。这三名患者均有BRCA突变并且都使用PARPi1作为一线治疗(表2)。
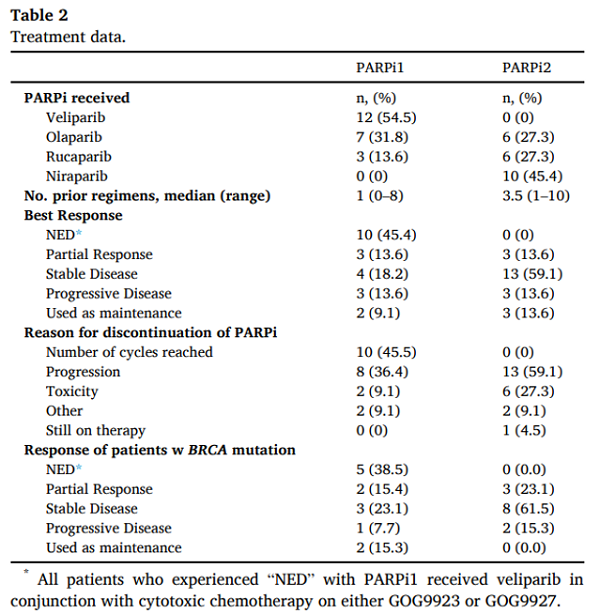
按BRCA状态细分时,BRCA突变人群使用PARPi复发治疗时有3例患者达到PR、8例疾病稳定(SD)和2例疾病进展(PD)。这似乎是应该在该人群中对PARPi进行rechallenge的信号(表2)。3例患者接受PARPi2维持治疗。在这3名患者中,1名患者在3个月时进展,1名患者尚未进展,最后1名患者在24个月时仍在接受治疗。
PARPi2因PD (n = 13)或毒性(n = 6)而停用。一名患者目前仍在接受PARPi2治疗(表2)。
8名患者因疾病进展而停用PARPi1。最佳应答中有:2名PR、2名SD、3名PD,1名患者由于使用PARP维持治疗不能作为评估。在这些患者中,对PARPi2的最佳应答为5 名SD和3名PD。最终,这些患者因疾病进展 (n =6)和毒性(n = 2) 而停用PARPi 2。尽管所有的8名患者都因疾病进展而中止了第1次使用PARPi,但仍有5名患者在第二次使用PARPi时以SD形式获得了临床获益。值得注意的是,这些应答是持久的,这5名患者中3名在PARPi2开始后保持无进展状态超过12个月(表3)。

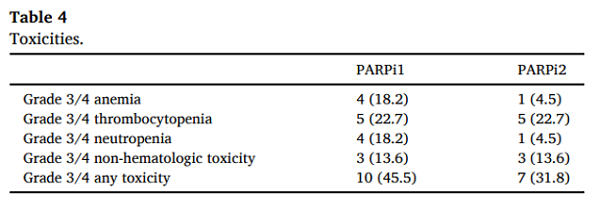
患者经历的最常见G3/4毒性为血液学毒性。初始使用PARPi后的毒性与第二次使用PARPi后的毒性无显著相关性(p > 0.05)。未发生AML/MDS(表4)。
4.讨论
这是一项小型研究,受到了人数少以及在不同一线治疗方案中接受PARPi治疗的限制。除了观察到患者对第2次PARPi暴露的反应之外,很难做出明确的结论。由此,我们得出结论,前线使用PARPi不一定会对后续使用PARPi产生耐药,在复发情况下似乎是一种安全的选择。一些患者能够从使用PARPi再治疗中获益,特别是把PARPi1作为一线治疗时疾病未进展的BRCA突变的肿瘤患者。此外,接受PARPi1治疗直至进展的患者对PARPi2治疗应答产生了一定的临床获益,这表明耐药性的产生不一定与先前的PARPi使用和疾病进展相关。此外,初次使用PARPi后的毒性与第二次使用PARPi后的毒性无显著相关性。毒性与PARPi2无关,表明安全性可以接受。
2019年9月,三项主要III期临床试验的结果显示,一线治疗后使用PARPi维持治疗有显著获益,最终获得FDA批准(Coleman,2019;Gonzalez- Martín,2019年;Ray-Coquard,2019年)。因此,越来越多的患者将在一线使用PARPi;由于卵巢癌患者高复发率,将需要更多有关再治疗疗效的数据。我们需要辨别哪些患者能从再治疗中获益的患者,并确定在应对获得性PARPi耐药性时,使用单一疗法与联合疗法哪个更好。目前,前瞻性随机对照试验OReO/ENGOT Ov-38试验(olaparib在铂敏感复发性卵巢癌中的再治疗)正在研究PARPi之后再使用PARPi的单一疗法问题。这项研究于2017年开始,预计初次数据公布会在2021年11月。
OReO将回答一个重要问题,但其他问题仍然存在,包括我们是否可以预测重复使用PARPi可能受益的患者,以及我们是否可以使用联合疗法来克服获得性铂耐药。我们目前的研究表明,既往使用PARPi疾病无进展的患者,可能只有BRCA突变的患者可从重复使用PARPi中获益;然而,鉴于本研究的局限性,暂时不能做出明确的结论。最近Rimel等人的研究也报告了类似的发现。他们发现在的niraparib ≥4线治疗的QUADRA研究中纳入的463名患者中,37名患者之前接受过PARPi治疗(Rimel,2020)。其中,23例(62%)为BRCA突变EOC,30例(81%)为HRD+,11例(30%)为铂敏感。33名患者(89.2%)在先前的PARPi治疗中出现疾病进展,客观缓解率 (ORR)为6%;然而,16周时的临床受益率(CBR)为20%,这也是疾病得到控制的信号。
目前正在确定可从PARPi再治疗中获益的患者的生物标志物。Pettitt 等人报告了导致PARPi耐药性的某些突变点(Pettitt,2018)。Lin等人报告了通过评估来自接受rucaparib治疗的患者的治疗前和治疗后血液样本中的循环细胞游离DNA (cfDNA)来识别BRCA逆转突变的能力(Lin,2019)。在需进行预处理活检的rucaparib的研究中,BRCA1甲基化纯合子患者似乎受益于rucaparib治疗,而甲基化杂合子患者似乎具有耐药性。纯合子丢失可能与既往化疗暴露(以及潜在的PARPi)有关,并可能作为PARPi再治疗敏感性的另一个潜在生物标志物(Kondrashova,2018)。
除了识别生物标志物外,重复使用PARPi可能需要联合治疗,以克服对PARPi的获得性耐药性。已有临床试验表明PARPi联合抗血管生成药物在治疗BRCAwt EOC有获益,表明PARPi和VEGF抑制剂的联合治疗可以克服固有的PARPi耐药性(Liu,2014;Mirza等人,。2019). 在Lheureux等人的一项研究中,34名既往使用PARPi疾病进展的患者接受了olaparib和cediranib治疗,ORR为12%。该研究确定了19例患者的耐药机制,包括BRCA1/2逆转(n = 4)、BRCA1/2过度表达(n = 1)、多药耐药蛋白过度表达(n = 2)、CCNE1扩增/过度表达(n = 6)和其他推断的机制(n = 6) (Lheureux等人,。2019). 早期数据证明了olaparib和α特异性PI3K抑制剂apelisib的安全性,也报告了疗效信号(ORR 36%),已被提议作为使用过PARPi的复发性EOC的可能组合(Konstantinopoulos,2019)。如果要重复使用PARPi,显然必须有多种基于特定耐药机制的组合方法。
总之,这是首次报告PARPi在既往使用过PARPi的复发性EOC患者中的使用情况的研究之一。虽然规模小且具有回顾性,但它确实证明了重复单一疗法的可能疗效,其确认有待OReO结果验证。重要的是,随着PARPi越来越多地用于早期治疗及BRCA相关癌症以外的治疗,越来越多的患者将出现PARPi既往使用,伴有/或不伴有PARPi后疾病进展。使用生物标志物选择合适疗法和进行合理联合以克服获得性耐药将是一个高需求且未得到满足的领域,需要继续进行进一步的研究。
参考文献:
Essel KG, Behbakht K, Lai T, Hand L, Evans E, Dvorak J, Ding K, Konecny G, Moore KN. PARPi after PARPi in epithelial ovarian cancer. Gynecol Oncol Rep. 2021 Jan 11;35:100699. doi: 10.1016/j.gore.2021.100699. PMID: 33537389; PMCID: PMC7840844.

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
