ICON8研究全文于2019年11月29日发表于《The Lancet Oncology》,研究共纳入1566例晚期卵巢癌患者,评估了紫杉醇周剂量密集化疗作为一线化疗的疗效和安全性。结果显示,与标准三周疗相比,两种周剂量密集化疗方案均没有延长患者PFS,但耐受性良好。2020年12月22日,《The Lancet Oncology》刊登了一篇题为《Objective responses to first-line neoadjuvant carboplatin–paclitaxel regimens for ovarian, fallopian tube, or primary peritoneal carcinoma (ICON8): post-hoc exploratory analysis of a randomised, phase 3 trial》的文章,本文为ICON8事后探索性分析一线新辅助化疗客观应答对PFS的影响,本期特别邀请来自中国科学院大学附属肿瘤医院(浙江省肿瘤医院)妇瘤外科陈曦医生对该研究进行解读。

中国科学院大学附属肿瘤医院
浙江省肿瘤医院妇瘤科副主任医师
浙江大学肿瘤学硕士
近年来以第一作者发表SCI论文5篇,主持卫生厅课题,参与省自然科学基金多项。主要从事妇科恶性肿瘤的手术治疗和化疗。

 00:000:00 音频
00:000:00 音频 1.研究背景
在国际妇产科学联合会(FIGO) III-IV期卵巢癌研究中,为新辅助化疗和DPS提供了明确的证据,但使用RECIST 1.1版和癌症抗原125 (CA125)评价新辅助化疗的反应率未见报道。
ICON8研究中意向治疗人群的初步无进展生存期分析显示,标准三周卡铂+紫杉醇与三周卡铂+周紫杉醇及周卡铂+周紫杉醇在无进展生存期方面没有显著差异。ICON8研究允许计划接受新辅助化疗后行DPS的患者参加试验,在这些患者中,使用RECIST 1.1和GCIG(Gynecologic Cancer InterGroup) CA125对新辅助化疗的应答进行了前瞻性评估。这项ICON8研究的事后探索性分析旨在调查新辅助化疗的客观应答是否影响无进展生存期和细胞减少率,是否可用于预测患者生存和DPS的有效性,从而指导手术治疗决策。
2.研究方法
ICON8是一项国际性、多中心、随机3期临床试验,在英国、澳大利亚、新西兰、墨西哥、韩国和爱尔兰等117家医院进行。这项探索性分析只包括ICON8研究中计划进行新辅助化疗并伴有DPS、且RECIST和/或CA125可评估的患者,无进展生存期采用里程碑式的方法进行分析,其定义为从术前计划影像学肿瘤评估日期到研究者评估临床或影像学进展或死亡日期(最先发生者)的时间间隔。这一定义与ICON8的意向治疗原发性无进展生存期分析不同,后者将无进展生存期定义为从随机分组到首次临床或影像学进展或死亡(最先发生者)的时间。另外,还比较了RECIST和CA125是否应答对手术细胞减少的影响程度。(ICON8已关闭注册和随访,并已在ClinicalTrials.gov上注册,NCT01654146。)
3.研究结果
PART-1
事后探索性分析的研究概要
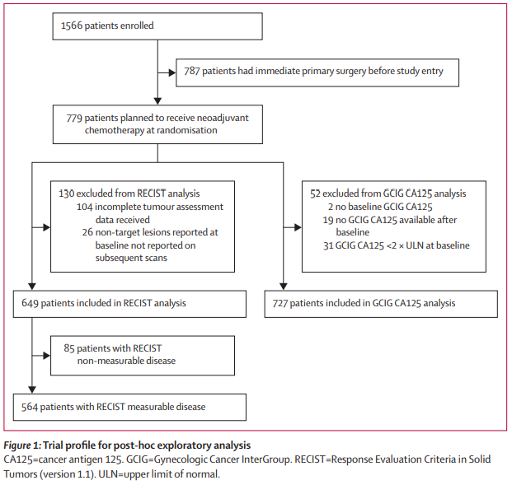
从2011年6月6日到2014年11月28日,ICON8研究共入组1566名患者。其中有779名(50%)计划接受新辅助化疗后行DPS,这组患者的中位随访时间为29.5个月(IQR为15.6-54.3)。纳入RECIST分析的患者为649名,其中564名(87%)患者有可测量的疾病。纳入CA125分析的患者有727名(93%)。
PART-2
新辅助化疗的RECIST应答与GCIG CA125应答
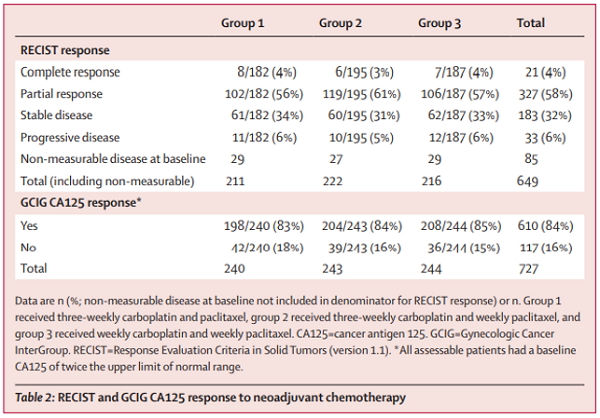
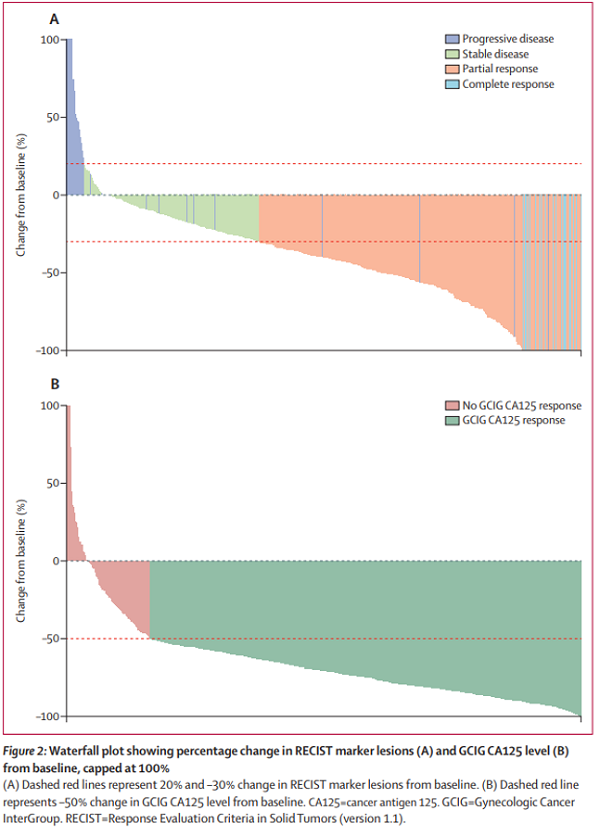
RECIST应答分析显示,348名(62%)患者新辅助化疗后有RECIST完全或部分应答,各个治疗组之间应答患者的比例没有差异(表2);有33名(6%)患者在新辅助化疗期间进展;另外,183名RECIST疾病稳定的患者中有156名(85%)患者标记病灶减小,平均减小了14% (IQR 5-23;图2 a)。
GCIG CA125应答分析显示,610名(84%)患者对新辅助化疗有CA125应答,各个治疗组间应答者的比例没有差异(表2;图2 b)。
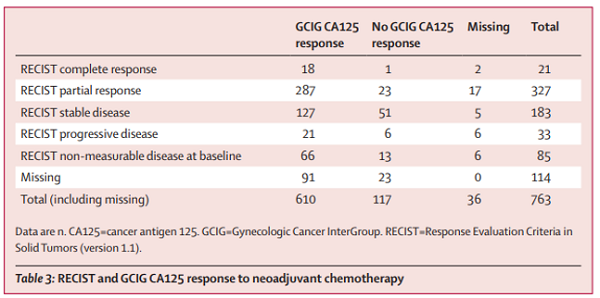
RECIST和GCIG CA125均有应答数据的患者有534名(表3)。存在GCIG CA125应答的患者中,有相当一部分没有RECIST应答:453名有GCIG CA125应答的患者且有RECIST评估的患者中,148名(33%)RECIST疾病稳定或疾病进展(表3)。同样这453名患者中,422名(93%)患者的标记病灶有减小。
PART-3
根据RECIST应答和CA125应答的PFS分析
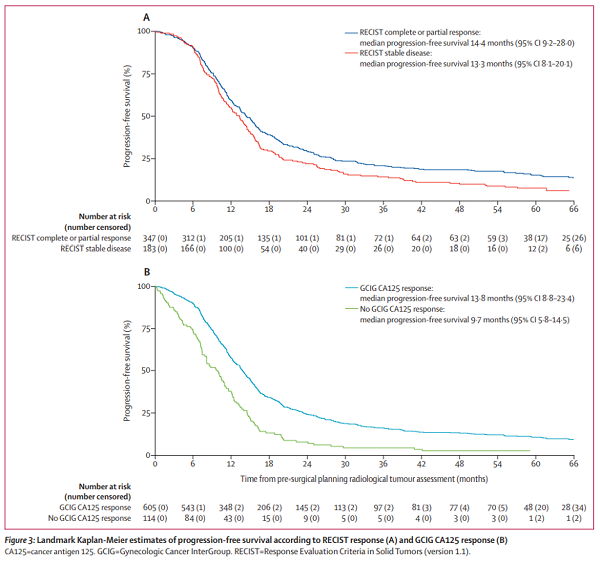
RECIST完全或部分应答的患者的中位无进展生存期为14.4个月(95% CI为9.2-28.0;297个事件),而RECIST疾病稳定的患者中位无进展生存期为13.3个月(95%CI为8.1 – 20.1;171个事件) (图3A)。(值得注意的是,使用里程碑式分析确定的生存期比意向治疗的主要疗效分析报告的生存期大约短2个月)。
GCIG CA125有应答的患者中位无进展生存期(里程碑分析)为13.8个月(95% CI为8.8- 23.4;544个事件),CA125没有应答的患者中位无进展生存期为9.7个月(95% CI为5.8-14.5;111个事件)(图3B)。
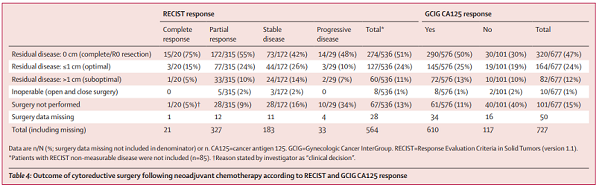
在564名RECIST可评估的患者中,有536(95%)人获得了手术结果数据,其中67名(13%)患者没有接受DPS(表4)。如果只包括那些接受了DPS的女性,RECIST完全或者部分应答的患者中位无进展生存期为15.0个月(95% CI 9.5 – 28.0,273个事件); RECIST疾病稳定的患者无进展生存期为14.0个月(95% CI 9.5-23.8;143个事件) 。130名影像学随访数据不完整的妇女中位无进展生存期短于(12.5个月,95% CI 7.5 – 17.2;118个事件)拥有完整的RECIST可评估影像学数据集的649名女性(15.4个月,95% CI 10.1-25.3;584个事件)。
RECIST可评估的患者在新辅助化疗后进行DPS的人群,中位无进展生存与手术细胞减灭程度相关,并且那些完全细胞减灭术(R0)的患者拥有最佳的中位无进展生存期,不论其对新辅助化疗的RECIST应答如何。在172名接受新辅助化疗后RECIST疾病稳定患者中,有73名(42%)患者的细胞完全减灭,尽管这一比例明显低于接受新辅助化疗RECIST完全或部分缓解患者(56%;表4;p=0.0040)。29例RECIST疾病进展的患者中有14例(48%)细胞完全减灭(表4)。
727例GCIG CA125可评估疾病的患者中,有677例(93%)患者获得了手术结果数据,其中101例没有经历过DPS(表4)。如果只包括那些经历了DPS的女性,CA125应答的患者中位无进展生存期为14.2个月(95% CI 9.3 – 25.0;490个事件),而CA125无应答的患者中位无进展生存期为10.5个月(95% CI 6.6 – 15.6;73个事件)。576例GCIG CA125有应答的患者中有290例(50%)达到了完全细胞减灭,101例没有应答的妇女中有30例(30%)达到了完全的细胞减灭(表4;χ2检验GCIG CA125反应与无反应比较,p<0·0001)。101例GCIG CA125无应答的妇女中有40例(40%)未做DPS,而576例GCIG CA125应答的妇女中仅有61例(11%)未做DPS(表4;χ2检验GCIG CA125反应与无反应比较,p<0·0001)。
为了确定结合两种常规疗效评估模式的结果是否能确定不太可能从DPS获益的患者群体,根据GCIG CA125疗效评估了RECIST稳定疾病患者的完全细胞减少率。完全细胞减少率与其他手术结果比较无明显差异(χ2检验比较完全细胞减少率与其他手术结果,p=0.18)。然而,值得注意的是,RECIST疾病稳定的患者且GCIG CA125有应答的患者经历手术多于RECIST疾病稳定但是没有GCIG CA125应答的患者 (109/121(90%) vs 32/47(68%))。
新辅助化疗后进行DPS的人群在新辅助化疗和DPS期间发生的所有不良反应, RECIST完全或部分缓解的患者与疾病稳定的患者相比没有差异。
RECIST和/或GCIG CA125可测量疾病的非高级别浆液性患者数量太少,无法就每种组织学亚型之间治疗反应的差异做出任何明确的结论。
4.讨论
对FIGO IC-IV期上皮性卵巢癌患者一线含铂新辅助化疗治疗反应的探索性分析有几个关键发现。
1、高级别浆液性卵巢癌新辅助化疗后RECIST完全或部分缓解率约为60%。
该研究是首个也是唯一的报道含铂一线新辅助化疗在上皮性卵巢癌中RECIST反应的前瞻性证据。
2、一线含铂新辅助化疗后RECIST稳定的患者不应排除DPS。
RECIST部分缓解和疾病稳定的患者中位无进展生存期相似,接受DPS的RECIST疾病稳定的患者中有42%达到了完全的细胞减少。这一发现支持在所有有RECIST完全缓解、部分缓解或稳定疾病的女性中进行DPS,在接受DPS之前不要求对新辅助化疗有反应。
3、GCIG CA125标准不能充分记录新辅助化疗的反应。
尽管没有GCIG CA125应答的患者相比有CA125应答的患者预后更差,但是近一半(49%)没有CA125应答的患者在DPS中获得最佳细胞减灭,而在RECIST疾病稳定的患者中30%达到完全细胞减灭。因此,不应单独使用GCIG CA125标准来定义哪些患者可能适合DPS。
5.结论
RECIST定义的影像学应答率低于临床经常引用的应答率。RECIST和GCIG CA125对上皮性卵巢癌新辅助化疗的反应不应被用作个体预测标志物来对可能受益于DPS的患者进行分层,而应与患者接受细胞减灭术的临床能力结合使用。患者不应仅仅因为RECIST或GCIG CA125反应不足而拒绝手术。

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
