NORA研究是第一项在亚洲人群中开展的PARP抑制剂用于维持治疗的3期临床研究,同时也是第一项绝大多数患者使用尼拉帕利个体化起始剂量用药方案的前瞻性研究。该研究初步结果在2020年ESMO大会上作为口头报告公布,2021年1月在《肿瘤学年鉴》(Annals of Oncology)杂志上全文发表。今天我们邀请到该研究的第一作者吴小华教授来为我们详细解读这一研究。

吴小华 教授
主任医师、博士生导师
复旦大学附属肿瘤医院主任医师、博士生导师、妇瘤科主任
妇科肿瘤多学科综合治疗组首席专家
现担任中国抗癌协会妇科肿瘤专业委员会主任委员
中华医学会妇科肿瘤专业委员会常委
中国临床肿瘤学会(CSCO)理事
上海市抗癌协会理事
妇科肿瘤专业委员会主任委员
曾任IGCS教育委员会委员、亚太地区理事候选人;SGO国际委员会委员;美国西北大学医学院客座教授等。目前还担任Internatioanl Journal of Gynecological Cancer, Cancer Medicine, Journal of Gynecological Oncology等杂志编委。
1.研究背景
晚期卵巢癌一线标准治疗是最大程度的肿瘤减灭术+含铂化疗,一线含铂化疗的有效率在80%左右,然而大部分患者还是在2年内复发。对于铂敏感复发患者来说,含铂化疗仍是标准治疗,然而随后每次化疗疗效逐次减低,毒性逐次加重。
PARP抑制剂维持治疗可以延长铂敏感复发卵巢癌PFS和CFI,不论是否存在BRCA突变。在3期NOVA研究中,尼拉帕利用于铂敏感复发卵巢癌维持治疗,73%患者从300mg减量,大部分是因为治疗前3个月发生的血小板减少。回顾性RADAR分析显示基线体重<77 kg或 基线血小板计数 <150×103/μL患者平均尼拉帕利维持治疗剂量是207mg,而疗效不受影响。因此3期NORA研究在研究启动后很短的时间内做了方案修改,采用了尼拉帕利基于基线体重和血小板的个体化起始剂量(200mg或300mg),评估其在中国铂敏感复发卵巢癌患者维持治疗的疗效和安全性。
2.研究方法
这是一项在中国范围内30家医疗中心开展的随机,安慰剂对照,双盲3期临床研究,纳入了≥18岁病理确认的上皮性卵巢癌、输卵管癌、原发性腹膜癌,高级别浆液性或携带BRCA突变患者不限制病理类型。所有患者既往接受≥2线含铂化疗,倒数第二次化疗达到完全缓解(CR)或部分缓解(PR),且复发≥6个月。末次化疗因包含≥4个周期含铂化疗后达到CR或PR。入组患者在末次化疗结束后8周内随机化。前16例患者采用固定300mg/d起始剂量修改方案后,采用使个体化起始剂量(体重≥77 kg 且血小板 ≥150×103/μL300mg/d起始,体重<77 kg 或血小板 <150×103/μL200mg/d起始)。一个治疗周期为28天,患者接受治疗直至疾病进展,死亡,或出现不可耐受的毒性反应,研究主要终点是BICR评估的无进展生存期,次要终点包括CFI、 TFS、OS和安全性。
3.研究结果
在2017年9月26日至2019年2月2日之间,共有265名患者入组。除方案修改前16例患者接受300mg固定起始剂量,其余249例(94%)的患者采用了个体化起始剂量的用药方案。数据截至时(2020年2月1日),中位随访时间是15.8个月。患者基线特征在两组间是平衡的(Table 1)。

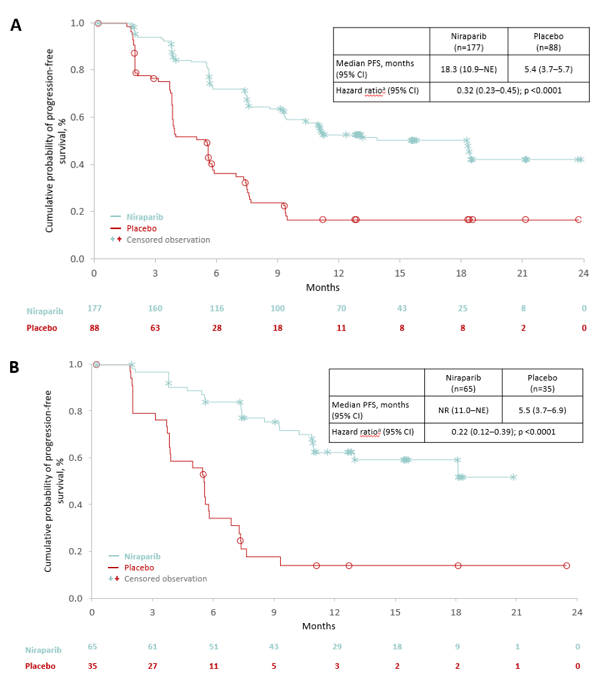
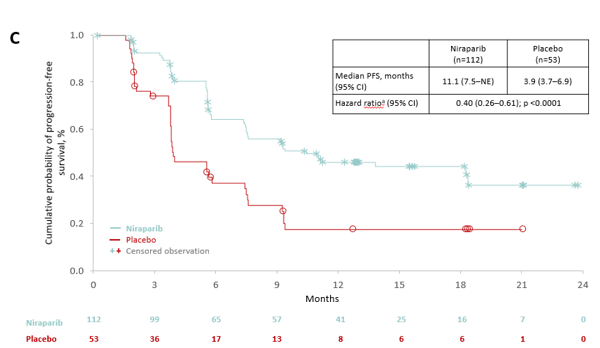
在ITT人群中,接受尼拉帕利患者疾病复发或死亡风险下降68%(HR=0.32; 95% CI, 0.23–0.45; p <0.0001)(图A),PFS较安慰剂组延长(18.3 [95% CI, 10.9?not evaluable] vs. 5.4 [95% CI, 3.7?5.7])。尼拉帕利组82 例(46.3%)患者疾病进展,安慰剂组67 例(76.1%)。不论BRCA基因突变状态,尼拉帕利组均有生存获益。胚系BRCA突变亚组PFS获益(not reached vs. 5.5 months; HR=0.22; 95% CI, 0.12–0.39)(图B),非胚系BRCA突变亚组PFS获益(11.1 vs. 3.9 months; HR=0.40; 95% CI, 0.26?0.61)(图C). 与主要终点结果相一致,次要终点分析显示尼拉帕利组患者中位CFI及中位TFST均较安慰剂组显著延长,(18.5 vs. 9.7 个月; HR=0.34; 95% CI, 0.24?0.48; p <0.0001),(16.7 vs. 7.7 个月; HR=0.35; 95% CI, 0.25?0.49; p <0.0001)。直至数据截止时,中位OS在两组均未达到。
安全性方面,尼拉帕利组最常见的任意级别治疗相关不良反应是血液学毒性,包括白细胞减少(59.3% vs. 43.2%),中粒细胞减少(58.8% vs. 42.0%),血小板减少(54.8% vs. 25.0% )和贫血(53.1% vs. 28.4%),最常见的任意级别的非血液学毒性包括恶心、呕吐和便秘(53.1, 32.2, 29.9%, vs. 19.3, 4.5, 10.2%)。尼拉帕利组最常见的3/4级血液学毒性是中性粒细胞减少,贫血和血小板减少。(20.3, 14.7, 11.3%, vs. 8.0, 2.3, 1.1% )。不良反应导致的剂量降低的发生率在尼拉帕利组和安慰剂组分别是59.9%和13.6%,因为绝大多数不良反应得到了充分的控制,极少数的患者最终因不良反应终止治疗,尼拉帕利组和安慰剂组因不良反应终止治疗的比例分别是4.0% 和 5.7%。
4.讨论和结论
这项研究是首个在亚洲患者群体中进行的PARP抑制剂维持治疗的随机3期临床试验,也是首个在此背景下评估个体化起始用药方案的前瞻性研究。主要终点分析显示尼拉帕利显著延长患者无进展生存期(HR=0.32),次要终点CFI和TFST也显示了与之相一致的结果,OS数据尚未成熟。研究表明尼拉帕利维持治疗对中国铂敏感复发性卵巢癌患者有效且耐受性好,为个体化起始剂量的临床应用提供了依据。
5.专家点评
NORA研究是第一项PARP抑制剂用于中国卵巢癌患者维持治疗的III期临床研究。该研究的结果为中国卵巢癌维持治疗临床实践提供了更夯实的循证医学依据。与此同时,该研究也是第一项绝大部分(94%)的患者使用尼拉帕利个体化起始剂量用药方案的前瞻性临床研究,为全球使用尼拉帕利患者的起始剂量选择提供了更多的理论依据。尼拉帕利个体化起始剂量用于铂敏感复发卵巢癌维持治疗也将成为中国卵巢癌患者标准治疗之一。


扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
