
刘淑娟 教授
主任医师
医学博士
西京医院妇产科副主任,副教授
中华医学会妇科肿瘤分会青年委员
陕西省抗癌协会宫颈癌防治专业委员会主任委员
中国医疗器械行业协会妇产科专委会副主委
全军妇产科专业委员会妇瘤学组委员
陕西省性学会妇瘤专委会副主委
中国优生协会肿瘤生殖分会常委
西安市医学会妇科分会常委

 00:000:00 音频
00:000:00 音频 1、背景
目前在肿瘤领域,PARP抑制剂备受关注,相关的基础及临床研究层出不穷。研究的焦点包括了在多个瘤种的尝试、使用时机的探索、联合策略的验证,除此之外,相关生物标记物也是研究的热点。选择有效的生物标志物对患者用药获益进行分层,实现个体化治疗,对临床医生和患者都具有重要价值 。
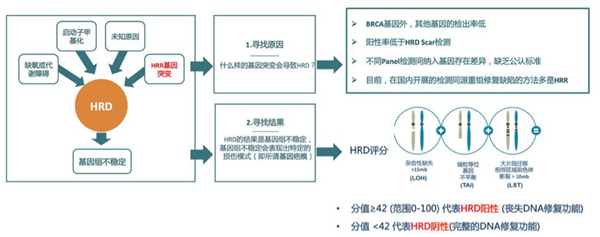
其中最受关注的是同源重组修复缺陷(homologous recombination deficiency,HRD)的检测,检测手段包括HRD评分、同源重组修复(homologous recombination repair, HRR)基因检测、基因组标签等,这些检测手段从技术上来说各不相同。
我们知道任何生物标记物都需要经过足够的临床验证,那么HRD几种检测手段的临床验证结果是否也不一样呢?目前常用的HRD的检测手段(HRR基因检测及HRD评分),是否足够用于指导PARP抑制剂的使用呢?2019年ASCO的一篇poster或许可以给我们带来一些思考。
2、方法
NOVA研究是一项尼拉帕利用于铂敏感复发卵巢癌患者维持治疗的国际多中心、随机双盲、前瞻性III期临床试验。
NOVA研究中非胚系BRCA突变(non-gBRCAmut)队列,无论患者通过Myriad myChoice HRD检测到的HRD状态如何,与安慰剂相比,尼拉帕利均能带来临床获益;HRD阳性患者风险比(HR)为0.38,HRD阴性患者HR为0.58。
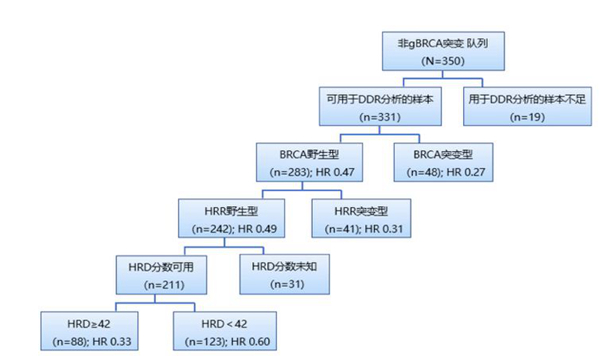
本研究对NOVA研究non-gBRCAmut队列中的331例患者的所有可用肿瘤样本,进行回顾性、探索性的生物标记物分析,以探索HRD评分及HRR基因突变的关系,以及不同人群的PFS。
HRD评分:Myriad myChoice HRD检测,评分≥42分定义为HRD阳性;
HRR基因检测:使用Myriad Genetics公司的DNA损伤修复基因(DNA damage repair, DDR)panel检测43个DDR基因中的有害突变,并重点分析其中18个HRR基因。18个HRR基因包括:BRCA1/2以及16个额外的HRR基因(ATM, BAP1, BARD1, BRIP1, MRE11A, NBN, PALB2, RAD50, RAD51B, RAD51C, RAD51D, RAD54B, RAD54L, ATR, XRCC2 和XRCC3)。
3、结果及讨论
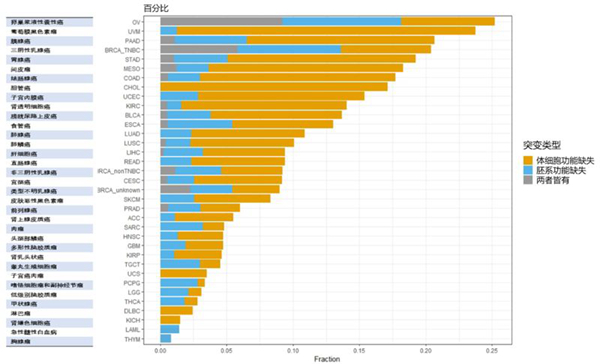
1. TCGA数据库数据分析示,卵巢浆液性囊腺癌中18个HRR基因突变率最高(功能缺失型突变约25%),此外胰腺癌、三阴性乳腺癌、胃腺癌、结肠腺癌、子宫内膜癌也存在18个HRR基因高突变(功能缺失型突变>15%)。
2. HRR基因检测与HRD评分的关系:
BRCA野生型中,HRR野生型占85%(242/283),HRR基因突变检出率仅为15%(41/283),提示HRR基因突变检出率偏低;
HRR野生型中,HRD阳性(HRD评分≥42)占36%(88/242),提示HRR基因野生型中仍有超过1/3 HRD高评分;

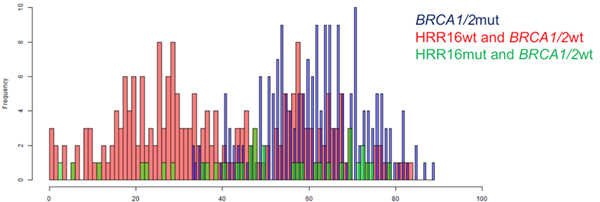
从HRD评分直方图中,可以更清晰地看到,虽BRCA突变(蓝色柱)主要分布于HRD高评分区域,但HRR wt(红色柱)和HRR16mut(绿色柱)在所有评分段均有分布。我们知道,HRD评分主要评估同源重组修复缺陷(HRD)带来的3种基因不稳定的分子指标,包括杂合性缺失(LOH)、端粒等位基因不平衡(TAI)和大片段重排(LST),评分≥42分则代表检测样本/患者存在同源重组修复缺陷(HRD);本研究结果显示即使检测出HRR基因有害突变,HRD评分仍可能较低,同时即使HRRwt,HRD评分仍可能高,提示检测HRR基因突变状态,并未能很好地预测同源重组修复缺陷的存在。所以HRRwt ≠ HRD<42分,HRRmut ≠ HRD ≥42分。
3. Biomarker临床验证结果:
基于NOVA研究的回顾性分析, sBRCAmut患者(HR 0.27)与BRCAwt/HRRmut患者(HR 0.31)相比,尼拉帕利维持治疗的临床获益相当;
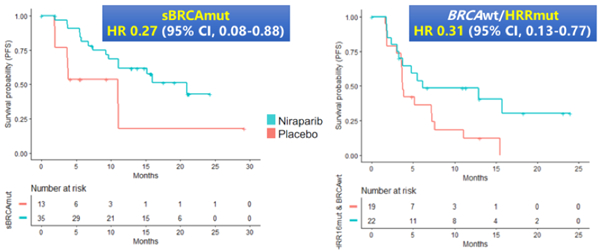
NOVA研究中non-gBRCAmut队列的探索性分析显示, sBRCAmut(HR 0.27)和BRCAwt(HR 0.47)患者均显示了临床获益,提示BRCA检测未能很好预测患者是否从尼拉帕利维持治疗获益;BRCAwt/HRRmut(HR 0.31)及 BRCAwt/HRRwt(HR 0.49)患者也均能从尼拉帕利的维持治疗中获益,提示HRR基因检测也未能很好预测患者是否从尼拉帕利维持治疗获益;
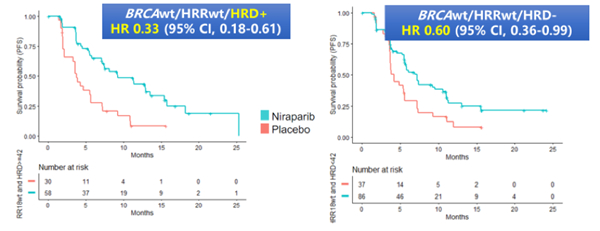
针对BRCAwt/HRRwt患者, 无论HRD阳性(HR 0.33)或HRD阴性(HR 0.60,95% CI 0.36-0.99)均有获益,提示HRD阳性(评分≥42)具有良好的阳性预测价值,HRD阳性患者从尼拉帕利治疗中获益明确,且与sBRCAmut(HR 0.27)与BRCAwt/HRRmut(HR 0.31)相似,但HRD阴性并不是好的阴性预测因子,HRD阴性(评分<42)并不代表患者不能从尼拉帕利治疗中获益。
4、总结
1. HRR基因检测≠HRD评分,检测HRR基因突变状态,并未能很好地预测同源重组修复缺陷的存在;
2. HRD相关生物标记物(BRCA基因、HRR基因、HRD评分)具有良好的阳性预测价值,但并不是尼拉帕利用于铂敏感复发性卵巢癌维持治疗获益的良好阴性预测因子;
3. 此项NOVA研究中non-gBRCAmut队列的回顾性、探索性分析显示,没有HRR基因突变的HRD阴性患者也有临床获益(可能与卵巢癌尚未定义的其他基因组、表观遗传学或功能改变有关)。
参考文献:Mansoor R. M., et al. Elucidation of PARP inhibitor activity in BRCAwt recurrent ovarian cancer by HRR mutational gene profile analysis. 2019 ASCO poster#391.

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
