卵巢癌的致死率很高。为了提高对初始治疗的反应率,目前正在进行生物制剂与化疗相结合以及化疗后维持治疗等多项临床试验。今年发表在Gynecologic Oncology上的综述回顾了clinical trials.gov上近期和正在进行的III期临床试验,这些试验研究了PARP抑制剂、抗血管生成剂、免疫检查点抑制剂以及这些药物的联合,另外还包括腹腔热灌注化疗(HIPEC)。本期OC资讯邀请到河南省肿瘤医院的荣方方医生,为大家解读这些试验现有的数据。

荣方方 医生
主治医师
医学硕士
河南省肿瘤医院
河南省医学会妇科肿瘤分会青年委员
河南省图形图像人工智能妇科委员会委员
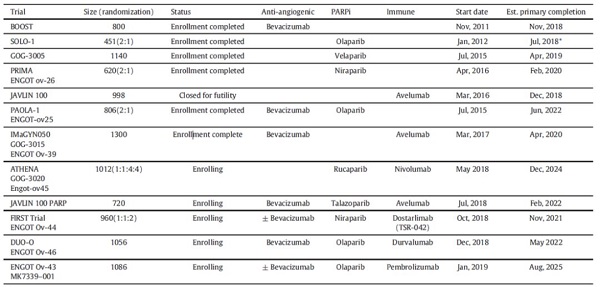
生物制剂与化疗结合的III期临床试验汇总

 00:000:00 音频
00:000:00 音频 1.抗血管生成药物
GOG 218是一项三臂、安慰剂对照的优效性试验,贝伐维持治疗组与标准化疗组的中位PFS分别为10.3个月和14.1个月,HR=0.72(95%CI :0.63-0.82,p<0.001)。进一步对CA125进展的患者进行亚组分析发现,中位的PFS从12.0个月增加到18.0个月, HR=0.65(95%CI:0.55-0.76,P<0.0001)。总的来说,贝伐单抗耐受性良好,但维持治疗组有22.9%的患者需要进行高血压治疗。
基于该试验的阳性结果,贝伐单抗先后被EMA(欧洲药品管理局)和FDA批准用于III/IV期卵巢癌术后联合化疗及化疗结束后的维持治疗。然而在美国,贝伐单抗并没有被迅速应用于一线。原因很可能在于成本、潜在的副作用和18个月的静脉输液,且PFS获益有限。在中位随访102.9个月后,2019年6月JCO公布了该研究的总生存OS结果:三组的中位OS分别为41.1个月、40.8个月和43.4个月。贝伐珠单抗同步-维持治疗组并未显示出生存优势。
ICON 7的结果与GOG 218相似,贝伐单抗组使得中位PFS从17.3个月增加到19.0个月, HR=0.81(95%CI:0.70-0.94,P=0.004)。但OS无获益。进一步分析显示,高危亚组应用贝伐后PFS获益更大,中位PFS从10.5个月增加到15.9个月,HR=0.70(95%CI:0.60-0.93,P=0.002)。中位OS从28.8个月增加到36.6个月, HR=0.64(95%CI:0.48-0.85,P=0.002)。高危亚组包括:FIGO III期且减瘤术后残留病灶>1cm或FIGO IV期患者。
BOOST试验(NCT01462890)将进一步优化贝伐单抗使用的最佳持续时间。该研究共纳入927例III/IV期原发性卵巢癌切除术后患者患者,按1:1随机分为使用贝伐单抗15个月和30个月。主要终点是PFS,次要终点包括客观反应率、OS、生活质量(QOL)和安全性。期待研究结果公布。
2.PARP抑制剂
目前,Niraparib、Olaparib和Rucaparib被批准用于铂敏感复发卵巢癌患者的维持治疗。在一线维持治疗方面,PARP抑制剂也有许多研究的探索。
SOLO-1研究结果在2018年ESMO公布,证明了Olaparib用于BRCA突变的晚期卵巢癌一线维持治疗的有效性。
PRIMA研究比较了Niraparib对比安慰剂维持治疗对初始化疗达CR/PR的患者的疗效(不论BRCA及HRD状态如何),纳入的人群包括III期PDS术后有残余病灶、接受新辅助化疗或无法手术的患者,排除了III期PDS术后达R0的患者。具体研究设计如下:

研究结果在2019年ESMO大会公布。与安慰剂组相比,尼拉帕利维持治疗显著延长同源重组修复缺陷(HRD)人群的PFS(21.9个月 vs 10.4个月),HR= 0.43 (95% CI:0.31–0.59,p<0.001);在总体人群中仍然取得阳性结果,相比安慰剂组降低38%复发或死亡风险,HR=0.62 (95% CI:0.50–0.76,p<0.001)。尼拉帕利是第一个证实一线含铂化疗后维持治疗,在不同生物标志物亚组中均有明确获益的PARPi。
从理论上讲,PARP抑制剂可以通过抑制肿瘤DNA亚致死损伤修复来增强化疗疗效。Veliparib在GOG 3005中将PARPi与含铂化疗联合,并在化疗结束后继续应用Veliparib进行维持治疗,对比标准化疗的生存获益。该研究证实了在BRCA突变患者中的生存获益,但与其他PARPi一线治疗的研究相比,联合化疗增加了毒性反应,并未增加获益。
3.免疫检查点抑制剂
PD-1抑制剂单药在未经筛选的卵巢癌患者中收效甚微。然而,在BRCA突变或其他可使新抗原负荷增加的情况下,应答率可能升高。卵巢癌的确可以表达新抗原,并且对于初始化疗达到完全缓解的患者,免疫治疗或许可以延长无病间期(disease free interval)和OS。尽管微卫星不稳定性高(MSI-H)的肿瘤占卵巢癌很少的一部分,但基于K药在MSI-H肿瘤中的适应症,K药获批用于MSI-H的卵巢癌。
JAVELIN系列试验探索了Avelumab联合化疗在卵巢癌中的应用。第一个报告结果的是JAVELIN 200,一项随机三臂临床试验。研究共纳入556例铂耐药或铂难治性患者。三组分别为聚乙二醇脂质体阿霉素(PLD)、Avelumab及两药联合。缓解率分别为4.2%、3.7%和13.3%。然而,该试验未达到预设的PFS和OS终点。
JAVELIN 100(NTC02718417)是一项III期国际多中心的试验,探索Avelumab同步或序贯含铂化疗在未经治疗的高级别、非粘液性晚期卵巢癌患者中的疗效和安全性。该研究入组了998例患者,但因期中分析未得出阳性结果于2018年12月提前终止。
4.联合治疗
目前有许多理论和试验证据支持生物制剂的联合可以发挥协同作用,且没有叠加的毒性。
缺氧是抗血管生成药物和PARP抑制剂联合产生协同作用的机制。在缺氧肿瘤组织中,控制同源重组修复的基因表达被抑制。PAOLA-1研究对比了贝伐用于一线维持治疗时,加或不加Olaparib的疗效。研究达到了主要终点,在总体患者中联合组PFS优于贝伐单药组(22.1个月 vs 16.6个月,HR=0.59),而在HRD阴性或状态未知的亚组并未观察到两组的疗效差别(16.9个月 vs 16.0个月,HR=0.92)。
血管生成信号的作用并不局限于血管生长,已有研究证明抗VEGF制剂可增强树突状T细胞的启动、减少调节性T细胞并增强免疫细胞肿瘤浸润。尽管有研究表明免疫抑制巨噬细胞可能通过抗VEGF治疗进入微环境,但贝伐单抗和免疫肿瘤药物的联合也可能具有协同作用。
PARP抑制剂与免疫检查点抑制剂的联合也可能产生协同。PARP抑制剂可以增加DNA损伤,导致胞浆DNA浓度增加,并激活STING途径,从而增加肿瘤的免疫原性。临床证据也支持这种联合的协同作用:TOPACIO是一项纳入62例晚期铂耐药卵巢癌患者的I/II期临床试验,证实尼拉帕利联合K药的有效率为25%-30%,且与BRCA或HRD状态无关。
5.腹腔热灌注化疗
腹腔内(IP)治疗在3个试验中显示了PFS和OS的优势。然而,由于毒性和新型化疗药物的发展进化,腹腔内化疗并未广泛应用。
GOG 172是2006年发表的里程碑式的腹腔内治疗的研究。腹腔紫杉醇联合顺铂化疗组将PFS从18.3个月(静脉化疗组)延长到23.8个月(HR=0.80,P=0.03)。总生存期从49.7个月增加到65.6个月(HR=0.75,P=0.05)。然而,3-4级恶心和呕吐、肾脏毒性、神经毒性等显著增加。
GOG 252是一项多中心三臂研究,卡铂、紫杉醇静脉治疗vs卡铂腹腔化疗联合紫杉醇静脉治疗vs顺铂+紫杉醇腹腔化疗联合紫杉醇静脉治疗,每组均加入贝伐珠单抗。但GOG 252未能达到改善PFS的主要终点,三组PFS分别为26.8个月,28.7个月和27.8个月。且腹腔组≥3级感染的发生率高于静脉组(17% vs 11.5%,p=0.008)。
一项145例患者的随机试验显示,接受新辅助化疗、间歇肿瘤细胞减灭术和术中HIPEC治疗的患者相比标准治疗组具有生存获益,;两组平均无复发生存期分别为14.2个月和10.7个月。HIPEC组的OS也从33.9个月提高到45.7个月。
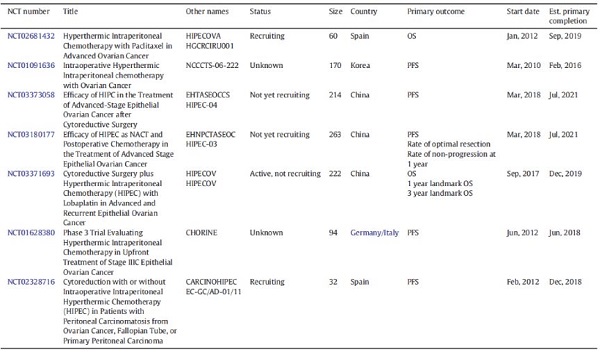
然而,腹腔内治疗观察到PFS的改善与初始化疗中加入贝伐单抗的获益相似。HIPEC在卵巢癌初始治疗中的作用仍不明朗。一些III期临床试验正在进行中,可能有助于确定HIPEC的最佳获益人群。
正在进行的HIPEC治疗原发性卵巢癌的试验
专家点评
基于GOG 218研究,贝伐单抗获批用于III-IV期存在高危因素的卵巢癌患者的一线维持治疗,但临床获益较为有限。SOLO-1研究证实了奥拉帕利在BRCA突变患者一线维持治疗的有效性,PRIMA研究中尼拉帕利再次证明PARPi在BRCA突变患者一线维持治疗的有效性,并进一步将维持治疗的获益扩大到HRD阳性甚至All-comer人群。
目前很难预测在一线治疗方案中加入免疫治疗的益处,这些药物在卵巢癌中的总有效率并不高。然而,免疫治疗获益的患者有可能产生长期的应答。哪些患者可能对免疫治疗有效?包括BRCA突变、HRD或其他高突变负荷或肿瘤免疫原性增加的情况下,联合用药可能具有协同作用。
正在进行的卵巢癌试验无疑带来巨大的希望,我们热切期待这些研究的结果。这些研究结果有望改变未来卵巢癌一线治疗的格局。

扫二维码
关注OC资讯

OC资讯小助手
为您提供更多帮助
